题目内容
10.下列反应属于分解反应的是( )| A. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | B. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
分析 分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”;据此进行分析判断.
解答 解:A、2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl,该反应符合“多变一”的特征,属于化合反应,故选项错误.
B、Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O,该反应符合“一变多”的特征,属于分解反应,故选项正确.
C、2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项错误.
D、AgNO3+NaCl═AgCl↓+NaNO3,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误.
故选:B.
点评 本题难度不大,掌握分解反应的特征(“一变多”) 并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
20.科学家用滤纸和二氧化钛(TiO2)制得纳米纸,在纳米纸上铺一层萘胺(C10H9N)又制得一种试纸,可用于检测食品中亚硝酸盐浓度的高低.下列说法正确的是( )
| A. | 这种试纸是一种新型化合物 | |
| B. | 二氧化钛中钛元素的化合价为﹢2 | |
| C. | 萘胺中氢元素的质量分数最小 | |
| D. | 萘胺是由10个碳原子、9个氢原子和一氮原子构成 |
1.下列物质在充满氧气的集气瓶中燃烧,产生明亮的蓝紫色火焰的是( )
| A. | 铁丝 | B. | 硫粉 | C. | 木炭 | D. | 红磷 |
1.A、B、C、D表示4种物质,其微观示意图如表.A和B在一定条件下反应可生成C和D,对该反应,下列说法不正确的是( )
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 | 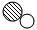 |  |  | |
| A. | 4种物质均由分子构成 | B. | 反应前后各元素化合价均发生改变 | ||
| C. | 4种物质中属于氧化物的是A、B、C | D. | C、D两种物质的质量比为22:7 |
18.下表中,除去物质所含杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 所选用试剂或方法 |
| A | CuO | Cu | 滴加足量盐酸,然后过滤 |
| B | CO2 | CO | 将气体通过灼热的氧化铜 |
| C | HCl | 水蒸气 | 将气体通过生石灰 |
| D | NaCl溶液 | Na2CO3 | 加适量的氢氧化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.某同学取回矿石样品,他对样品中的碳酸钙的质量分数进行检测,方法是:取矿石样品8g,将40g盐酸溶液分四次加入,所得数据如下表(已知石灰石样品中的杂质不溶于水,不与盐酸反应)请计算:
(1)如表中m的数值3;n的数值1.2.
(2)样品中碳酸钙的质量分数?
(3)要制取4.4g二氧化碳,需纯碳酸钙多少克?
| 序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
| 1 | 10 | 5.5 |
| 2 | 10 | m |
| 3 | 10 | 1.2 |
| 4 | 10 | n |
(2)样品中碳酸钙的质量分数?
(3)要制取4.4g二氧化碳,需纯碳酸钙多少克?