题目内容
1.下列物质在充满氧气的集气瓶中燃烧,产生明亮的蓝紫色火焰的是( )| A. | 铁丝 | B. | 硫粉 | C. | 木炭 | D. | 红磷 |
分析 A、根据铁丝在氧气中燃烧的现象进行分析判断.
B、根据硫粉在氧气中燃烧的现象进行分析判断.
C、根据木炭在氧气中燃烧的现象进行分析判断.
D、根据红磷在氧气中燃烧的现象进行分析判断.
解答 解:A、铁丝在氧气中剧烈燃烧,火星四射,故选项错误.
B、硫粉在氧气中燃烧,发出明亮的蓝紫色火焰,故选项正确.
C、木炭在氧气中燃烧,发出白光,故选项错误.
D、红磷在氧气中燃烧,产生大量的白烟,故选项错误.
故选:B.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
9. 如图所示,将盛有铁屑的量筒塞上蓬松的棉花,然后倒置在水中(固定装置已略去),数天后,可观察到的现象是( )
如图所示,将盛有铁屑的量筒塞上蓬松的棉花,然后倒置在水中(固定装置已略去),数天后,可观察到的现象是( )
 如图所示,将盛有铁屑的量筒塞上蓬松的棉花,然后倒置在水中(固定装置已略去),数天后,可观察到的现象是( )
如图所示,将盛有铁屑的量筒塞上蓬松的棉花,然后倒置在水中(固定装置已略去),数天后,可观察到的现象是( )| A. | 铁屑不生锈,量筒内液面上升 | B. | 铁屑不生锈,量筒内液面不上升 | ||
| C. | 铁屑生锈,量筒内液面上升 | D. | 铁屑生锈,量筒内液面不上升 |
10.下列反应属于分解反应的是( )
| A. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | B. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
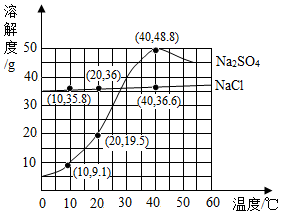 如图为Na2SO4和NaCl的溶解度曲线.下列叙述正确的是( )
如图为Na2SO4和NaCl的溶解度曲线.下列叙述正确的是( )
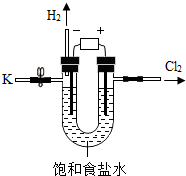 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分溶液作为待测液进行如下探究.(提示:可以忽略其他可能发生的反应对以下实验的影响;Mg(OH)2在水中不溶)
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分溶液作为待测液进行如下探究.(提示:可以忽略其他可能发生的反应对以下实验的影响;Mg(OH)2在水中不溶)