题目内容
14.图Ⅰ所示为甲、乙两种固体物质的溶解度曲线.常温下,盛水烧杯内的两试管中分别盛有甲、乙的饱和溶液,并都有少量固体存在,如图Ⅱ所示.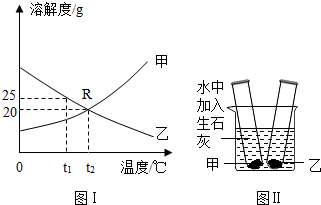
(1)请你写出图Ⅰ中R点的一条含义t2℃时,甲、乙物质的溶解度相等.
(2)将t1℃时甲、乙的饱和溶液升温到t2℃,所得两种溶液的溶质质量分数的关系是甲小于乙 (填“大于”、“小于”或“等于”).
(3)若饱和乙溶液的溶质质量分数为20%,此时乙所处的温度是t1.(填“t1”或“t2”)
(4)在图Ⅱ实验中,观察到试管中甲固体减少,乙固体增多.请你对此现象作出解释:氧化钙与水反应放出热量,甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高减小.
(5)小娜同学用某固体物质进行了如下图所示的实验,据此判断下列说法错误的是C.
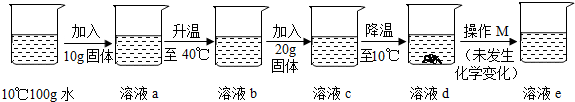
A.该固体物质的溶解度随温度的升高而增大
B.溶液b一定是不饱和溶液
C.溶液d中的溶质质量可能大于溶液e中的溶质质量
D.溶液d和溶液e的溶质质量分数可能相同.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,图Ⅰ中R点的一条含义是:t2℃时,甲、乙物质的溶解度相等;
(2)将t1℃时甲、乙的饱和溶液升温到t2℃,乙物质会析出晶体,但是乙物质t2℃时的溶解度大于甲物质t1℃时的溶解度,所以所得两种溶液的溶质质量分数的关系是甲小于乙;
(3)若饱和乙溶液的溶质质量分数为20%,乙物质的溶解度应该是25g,所以此时乙所处的温度是t1;
(4)在图Ⅱ实验中,观察到试管中甲固体减少,乙固体增多,对此现象作出解释是:氧化钙与水反应放出热量,甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高减小;
(5)A、从溶液c 和溶液d可以看出,降低温度则溶液中会析出晶体,说明该物质的溶解度随温度的升高而增大,故A正确;
B、溶液b中加入20g固体得到的溶液c中没有未溶解的固体,说明加入的物质全部溶解,故溶液b一定是不饱和溶液,故B正确;
C、溶液d变成溶液e的过程中没有发生化学变化,说明溶液d中的固体除掉,可能是升高温度使固体溶解,则溶液d中溶质质量可能大于溶液e中的溶质质量,故C错误;
D、若是溶液d中的固体是经过过滤除去,则溶液d和溶液e的溶质质量分数可能相同,故D正确;
故选:C.
故答案为:(1)t2℃时,甲、乙物质的溶解度相等;
(2)小于;
(3)t1;
(4)氧化钙与水反应放出热量,甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高减小;
(5)C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

| A. |  | B. |  蒸发溶剂 | C. |  取用药品 | D. |  |
| A. | -4 | B. | -2 | C. | +2 | D. | +4 |
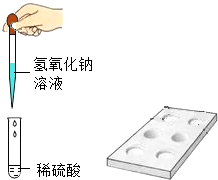 九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.
九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.【提出问题】这些同学试管中的“氢氧化钠与稀硫酸是否恰好完全反应”?
【猜想与假设】
A.恰好完全反应 B.硫酸过量 C.氢氧化钠过量
【实验探究】
甲、乙、丙、丁四名同学分别取四个不同样品于试管中,继续探究.
| 所用试剂 | 实验现象 | 实验结论 | |
| 甲同学 | 硫酸铜瘠液 | 产生蓝色沉淀 | 氢氧化钠过量 |
| 乙同学 | 氯化钡溶液 | 产生白色沉淀 | 硫酸过量 |
| 丙同学 | 锌粒 | 产生气泡 | 硫酸过量 |
| 丁同学 | 无色酚酞溶液 | 溶液不变色 | 恰好完全反应 |
(2)请你评价乙同学的实验结论不合理,硫酸钠能与氯化钡反应产生白色沉淀;
(3)丙同学实验时观察到的现象是产生气泡(写完整).
(4)大家一致认为丁同学的实验结论错误,他能得出的结论是:反应后的溶液可能呈酸性或是中性;
【反思与收获】
(5)若要证明一个化学反应是恰好完全反应的,应设计实验证明反应物是否剩余;
【拓展延伸】
(6)溶液之间的反应可以根据需要选择“烧杯、试管、点滴板”等作为反应容器,三者比较,点滴板的优点是节约药品(写一点).
| A. | CaO+H2O→Ca(OH)2 | B. | 2H2O→2H2↑+O2↑ | ||
| C. | 4Fe+3O2$\stackrel{点燃}{→}$2Fe2O3 | D. | Zn+HCl→ZnCl2+H2↑ |
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】I.只有氧化钙
II.只有碳酸钙
III.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想II成立.乙同学认为上述实验不足以证明猜想II成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想III成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,过滤,取滤液滴加无色酚酞溶液 ②取滤渣滴加足量的稀盐酸 | 溶液变红色 有气泡产生 | 猜想 III成立 |
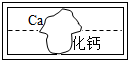 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M物质的溶质有两种可能:
①是氢氧化钙 ②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加 酚酞 | 溶液变红 | 猜想①正确 |
【提出猜想】猜想一:NaOH 和Na2CO3; 猜想二:NaOH和Ca(OH)2;猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入两滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
若A中没有沉淀,B中产生沉淀 | “猜想二”成立 | |
若AB中都没有沉淀 | “猜想三”成立 |