题目内容
12.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律,如图是元素周期中1-18号元素原子核外电子排布.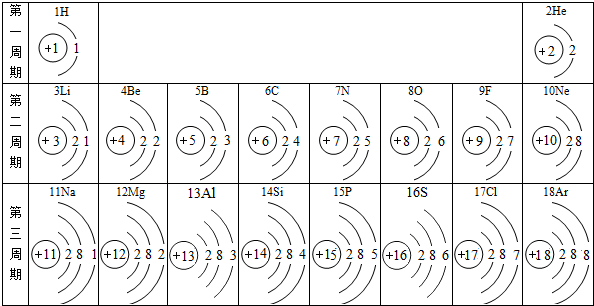
(1)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,同一周期元素原子的电子层数相同.
(2)11号元素属于金属元素(填“金属”或“非金属”),它在化学反应中形成的离子与Ne(写元素符号)原子具有相同的核外电子排布.
(3)表中每一个横行叫做一个周期,每一个纵行叫做一个族.
分析 (1)根据元素周期表中同一周期的规定来分析;
(2)根据已有的知识进行分析,钠元素属于金属元素;
(3)表中每一个横行叫做一个周期,每一个纵行叫做一个族
解答 解:(1)第二周期的3-10号元素原子的电子层数相同,第三周期的11-18号元素原子的电子层数也相同,因此得出规律每一周期元素原子的电子层数相同;
故答案为:电子层数;
(2)11号元素是钠元素,属于金属元素,失去电子后,形成的钠离子与氖原子具有相同的核外电子排布;
故填:金属,Ne;
(3)表中每一个横行叫做一个周期,每一个纵行叫做一个族;
故填:族.
点评 本题考查了元素周期表的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案
相关题目
20.下列做法或说法中错误的是( )
| A. | 火场逃生时在有烟雾的地方应匍匐前进 | |
| B. | 为了防止水污染,农业上要合理使用化肥、农药 | |
| C. | 回收废旧电池,即可节约金属资源又可减少环境污染 | |
| D. | 人体缺锌会引起生长发育缓慢,因此锌元素的摄入量越多越好 |
7.只用一种试剂就可一次性鉴别稀硫酸,烧碱溶液、食盐溶液的是( )
| A. | 纯碱溶液 | B. | 酚酞试液 | C. | 石蕊试液 | D. | 稀盐酸 |
7.下列四种金属中,有一种金属能与其余三种金属的盐溶液反应,则该金属是( )
| A. | Mg | B. | Cu | C. | Fe | D. | Ag |
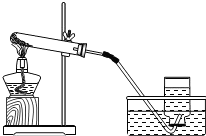 某同学在实验室用以下装置制备氧气并探究氧气的性质.
某同学在实验室用以下装置制备氧气并探究氧气的性质.