题目内容
2.在实验室配制溶液时,常涉及以下过程:①称量、量取②过滤③蒸发结晶干燥④计算⑤溶解
请按要求回答下列问题:
(1)甲同学用氯化钠和蒸馏水配制50g 5%的氯化钠溶液,正确的操作顺序是④①⑤ (用以上序号填空)
(2)现实验室中有10mL、50mL、100mL等不同规格的量筒,配制上述溶液时最好选用50mL的量筒.
分析 根据配置溶液的基本步骤考虑本题,根据量筒量程的选取方法来选择;
解答 解:
(1)配置一定质量分数氯化钠溶液的基本步骤是:计算、称量、量取、溶解;
(2)通过计算,需要氯化钠的质量是50g×5%=2.5g,需要水的质量是50g-2.5g=47.5g,由于水的密度是1g/cm3,所以需要量取的水的体积是47.5mL,量筒的量程的选取方法是选取比所量液体体积大,且最接近的因为需水47.5,所以选50mL的量筒;
故答案为:(1)④①⑤;(2)50.
点评 通过回答本题知道了配制溶液的步骤和配制溶液所需要的仪器选择方法,掌握了含杂质溶液配制的方法.

练习册系列答案
相关题目
13.镁与NH4Cl溶液反应,不仅有一种盐生成,还有气泡产生.为确定生成气体的成分,某化学小组的同学进行了如下实验探究.
【查阅资料】①NH3能与水反应生成NH3•H2O;②气体的溶解度随温度的升高而减小;③NH3+HCl═NH4Cl,2NH3+H2SO4═(NH4)2SO4;④NH4Cl溶液和(NH4)2SO4溶液均显酸性.
【提出问题】镁与NH4Cl溶液反应生成何种气体?
【猜想与假设】甲同学说:生成的气体可能是HCl、NH3、H2中的一种或几种.
甲同学提出上述猜想的理论依据是化学反应前后元素种类保持不变.
【进行实验】为了验证以上猜想,小组同学设计了如图装置进行实验:
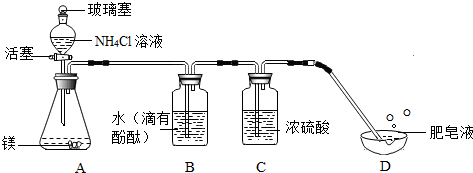
【现象与结论】
【反思与评价】
(1)有同学认为不需要单独检验HCl,就能证明HCl不存在,理由是因为氨气能和氯化氢反应生成氯化铵.
(2)C装置中浓硫酸的主要作用是吸收水蒸气和氨气.
(3)写出Mg与NH4Cl溶液反应的化学方程式:Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中A装置有氨气逸出的原因可能是该反应放热,温度升高,使氨气在水中的溶解度减小.
【查阅资料】①NH3能与水反应生成NH3•H2O;②气体的溶解度随温度的升高而减小;③NH3+HCl═NH4Cl,2NH3+H2SO4═(NH4)2SO4;④NH4Cl溶液和(NH4)2SO4溶液均显酸性.
【提出问题】镁与NH4Cl溶液反应生成何种气体?
【猜想与假设】甲同学说:生成的气体可能是HCl、NH3、H2中的一种或几种.
甲同学提出上述猜想的理论依据是化学反应前后元素种类保持不变.
【进行实验】为了验证以上猜想,小组同学设计了如图装置进行实验:

【现象与结论】
| 装置 | 实验现象 | 实验结论 |
| B | 溶液变红 | 生成的气体中含有氨气 |
| D | 肥皂泡飘到空气中,用燃着的木条靠近肥皂泡,有爆鸣声 | 生成的气体中含有 氢气 |
(1)有同学认为不需要单独检验HCl,就能证明HCl不存在,理由是因为氨气能和氯化氢反应生成氯化铵.
(2)C装置中浓硫酸的主要作用是吸收水蒸气和氨气.
(3)写出Mg与NH4Cl溶液反应的化学方程式:Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中A装置有氨气逸出的原因可能是该反应放热,温度升高,使氨气在水中的溶解度减小.
17.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2气体 | SO2 | 通入石灰水 |
| B | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| C | 炭粉 | CuO粉末 | 加入过量稀硫酸,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
14.下列物质中属于纯净物的是( )
| A. | 某品牌纯净水 | B. | 清新的空气 | C. | 石灰水 | D. | 蒸馏水 |

 A~N是初中学过的物质.D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀.实验室通常用N制CO2,如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.(注:难溶性碱加热分解生成对应的氧化物)
A~N是初中学过的物质.D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀.实验室通常用N制CO2,如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.(注:难溶性碱加热分解生成对应的氧化物)