题目内容
14. 厨房中有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种.小明对白色粉末的成分进行了探究.
厨房中有一包无标识的白色粉末,经初步认定可能是氯化钠、碳酸钠、碳酸氢钠中的一种.小明对白色粉末的成分进行了探究.【查阅资料】碳酸钠俗称苏打,碳酸氢钠俗称小苏打,两者都属于盐(选填“酸”、“碱”、“盐”),都能溶于水,且水溶液都呈碱性.
实验探究一、确定白色粉末的成分,小明取适量白色粉末,配制成溶液,按表中所示实验方案进行探究.
| 实验步骤 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是NaCl |
| 2 | 取少量溶液,滴加稀盐酸 | 有气泡产生 | |
| 3 | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 |
(2)实验步骤2中可能发生反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑(写出一个即可),实验步骤3中白色沉淀的成分是CaCO3(填写化学式).
【实验反思】小明实验后发现上述实验方案并不能确定白色粉末的组成.经老师指导后,小明再取少量配制的溶液滴加氯化钙溶液,没有观察到明显现象,确定该白色粉末为碳酸氢钠.
实验探究二、确定白色粉末的化学性质
(1)碳酸氢钠溶液的酸碱性:用pH试纸测得碳酸氢钠溶液的pH约为10,由此得出结论是碳酸氢钠溶液呈碱性.
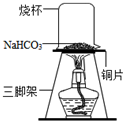
(2)碳酸氢钠的热稳定性:①取一定量的碳酸氢钠放在铜片上加热,如图所示加热一段时间后,观察到烧杯内壁有水珠.
②充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑浊
③通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| a | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙,振荡,静置 | 产生白色沉淀 | 产物含Na2CO3 |
| b | 取操作①后的上层清液于试管B中,滴加酚酞 | 溶液不变色 | 产物不含NaOH |
分析 实验探究一、由金属离子和酸根离子组成的化合物属于盐;
氯化钠溶液显中性,不能使酚酞试液变色;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳;
碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊.
实验探究二、(1)当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性.
(2)检验生成物是NaOH还是Na2CO3,加入氯化钙溶液可以与碳酸钠反应产生沉淀的物质,据此进行分析解答.
碳酸氢钠受热容易分解,生成水、二氧化碳气体和Na2CO3,写出反应的化学方程式即可.
解答 解:【查阅资料】
(1)碳酸钠俗称纯碱、苏打,碳酸氢钠俗称小苏打,两者都属于盐,都能溶于水,且水溶液都呈碱性,小苏打受热易分解产生二氧化碳.
故填:盐.
【实验探究】
实验过程如下表所示:
| 实验步骤 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是氯化钠 |
| 2 | 取少量溶液,滴加稀盐酸 | 产生气泡 | / |
| 3 | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 | / |
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑,或NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)实验步骤3中白色沉淀的成分是碳酸钙,碳酸钙的化学式是CaCO3.
故填:CaCO3.
实验探究二、(1)用pH试纸测得碳酸氢钠溶液的pH为10,大于7,显碱性;故填:碱性;
(2)检验生成物是NaOH还是Na2CO3,加入足量的氯化钙溶液可以与碳酸钠溶液反应产生沉淀的物质,若有白色沉淀生成,说明固体产物是Na2CO3取反应后的上层清液,向其中滴加酚酞试液,酚酞试液不变红,说明溶液中不含氢氧根,说明固体产物中不含氢氧化钠;故答案为:
| 序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量 氯化钙溶液,振荡,静置. | 产生白色沉淀 | 产物含Na2CO3 |
| ② | 取操作①后的上层清液于试管B中,滴加 酚酞试液. | 酚酞试液不变色 | 产物不含NaOH |
点评 本题综合考查了碳酸钠、碳酸氢钠的知识,回答问题时,可以依据课本已有的知识,灵活应用,所以同学们在平时的学习中要加强知识的理解与应用

练习册系列答案
相关题目
9.金属是一类重要的材料,人类生产、生活都离不开金属.下面是小海同学对铁的部分知识的学习、探究.
(1)小海对铁制品生锈情况的调查:
由上可知铁制品生锈是铁与空气中的氧气和水共同作用的结果.
(2)为证明铁的金属活动性比铜强,请与小海一起完成实验设计:
(1)小海对铁制品生锈情况的调查:
| 调查内容 | 涂油的无锈铁钉 | 炒菜的铁锅 | 土壤中的铸铁管道 |
| 铁制品锈蚀的现象 | 较长时间仍不生锈 | 清洗后,擦干置于干燥处,未生锈 | 在潮湿、疏松透气的土壤中生锈明显 |
(2)为证明铁的金属活动性比铜强,请与小海一起完成实验设计:
| 实验步骤 | 观察到的现象 | 反应的化学方程式 |
| 将铁片放入盛有少量硫酸铜溶液的试管中 | 铁片表面出现红色金属,溶液逐渐变为浅绿色 | Fe+CuSO4=FeSO4+Cu |
2.下列有关报道与事实不相符合的是( )
| A. | 由于中东地区的长期内战对水和空气的严重污染,使得近些年中东地区5岁以下儿童得死亡率大大增加 | |
| B. | 冬天使用煤炉的家庭容易发生一氧化碳中毒,而一氧化碳是无色无味的气体,这是容易发生一氧化碳中毒的主要原因之一 | |
| C. | 随着工农业生产的发展,人口的增加,淡水也不是取之不尽,用之不竭的 | |
| D. | 新粉刷过石灰浆的墙壁释放出二氧化碳,使一老汉窒息死亡 |
9.室温下,下列生成MgCl2的转化关系能通过一步反应实现的是( )
| A. | AgNO3→MgCl2 | B. | KNO3→MgCl2 | C. | NaCl→MgCl2 | D. | Mg(OH)2→MgCl2 |
19.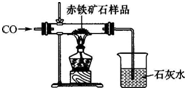 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(2)在利用上图装置进行实验时,小强得到如上两组数据(杂质不参加反应)
你认为他应该选用A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数;结合装置图回答他不能选用另一组数据计算的原因是石灰水也会吸收空气中的二氧化碳,导致数据m4有误差.
 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是2857t?(结果保留整数)| 反应前 | 氧化铁完全反应后 | |
| A组 | 玻璃管和赤铁矿石样品的质量m1g | 玻璃管和固体物质的质量m2g |
| B组 | 烧杯和澄清石灰水的质量m3g | 烧杯和烧杯中物质的质量m4g |
你认为他应该选用A(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数;结合装置图回答他不能选用另一组数据计算的原因是石灰水也会吸收空气中的二氧化碳,导致数据m4有误差.
6.物质与水发生的复分解反应称为水解反应.例如:Al2S3+6H2O═2Al(OH)3↓+3H2S↑.根据上述观点,下列说法中不正确的是( )
| A. | NaF的水解产物是NaOH和HF | B. | CaO2的水解产物是Ca(OH)2和C2H2 | ||
| C. | PCl3的水解产物之一是PH3 | D. | Mg3N2水解产物是Mg(OH)2和NH3 |