题目内容
8.采用控制变量法设计实验方案,以2min内收集到的氧气体积作为判断依据,具体如下表所示:| 实验序号 | 温度/℃ | H2O2溶液体积及浓度 | 催化剂 | O2体积/mL(均收集2min) |
| ① | 20 | 5mL、12% | 无 | V1 |
| ② | 60 | 5mL、12% | 无 | V2 |
| ③ | 20 | 5mL、4% | 无 | V3 |
| ④ | 20 | 5mL、12% | 0.5gCuCl2固体 | V4 |
(2)探究H2O2分解快慢受浓度的影响,其实验序号分别是①>③
(3)为继续探究是CuCl2中的Cu2+对H2O2分解具有催化作用,在实验④其它条件不变的情况下,用CuSO4代替CuCl2固体进行实验,即可得出正确结论.
分析 (1)四种情况下,均有气泡产生;
(2)根据过氧化氢分解的快慢与反应物浓度的关系来分析;
(3)选择一种能电离出铜离子的可溶性盐来代替.
解答 解:(1)可以根据产生气泡的快慢来判断;故填:产生气泡的快慢;
(2)在温度相同、没有催化剂的条件下,反应物的浓度越大,分解速率越快;故填:①>③;
(3)硫酸铜、硝酸铜也可以电离出铜离子,可用硫酸铜来代替,故填:CuSO4.
点评 本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案.

练习册系列答案
相关题目
19. A、B两种物质的溶解度曲线如图甲所示,在t1℃时,A、B两种物质配制溶液的情况如图乙所示,下列说法正确的是( )
A、B两种物质的溶解度曲线如图甲所示,在t1℃时,A、B两种物质配制溶液的情况如图乙所示,下列说法正确的是( )
 A、B两种物质的溶解度曲线如图甲所示,在t1℃时,A、B两种物质配制溶液的情况如图乙所示,下列说法正确的是( )
A、B两种物质的溶解度曲线如图甲所示,在t1℃时,A、B两种物质配制溶液的情况如图乙所示,下列说法正确的是( )| A. | t1℃时,两个烧杯内均有固体剩余,且质量相等 | |
| B. | 由t1℃到t2℃过程中,A溶液中溶质的质量分数减小 | |
| C. | t2℃时,烧杯中的A溶液为饱和溶液 | |
| D. | 由t2℃到t1℃,B的溶液中有晶体析出 |
3.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wuthrich等人为此获得2002年诺贝尔化学奖.下面有关13C、15N叙述正确的是( )
| A. | 13C与15N有相同的中子数 | B. | 13C与12C有相同的中子数 | ||
| C. | 15N与14N的核电荷数相同 | D. | 15N的核外电子数与中子数相同 |
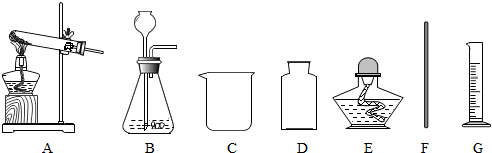
7.现有仪器烧杯、试管、广口瓶、铁架台、集气瓶、止水夹、酒精灯、玻璃片、燃烧匙、带导气管的橡皮塞,坩埚钳从缺少仪器的角度考虑,下列实验不能进行的是( )
| A. | 空气中氧气体积含量的测定 | B. | 制取氧气 | ||
| C. | 细铁丝在氧气中燃烧 | D. | 浑浊的水过滤 |
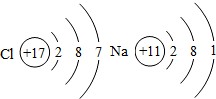 如图是两种元素的原子结构示意图.据此回答:
如图是两种元素的原子结构示意图.据此回答: