题目内容
3.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wuthrich等人为此获得2002年诺贝尔化学奖.下面有关13C、15N叙述正确的是( )| A. | 13C与15N有相同的中子数 | B. | 13C与12C有相同的中子数 | ||
| C. | 15N与14N的核电荷数相同 | D. | 15N的核外电子数与中子数相同 |
分析 13C、15N的质量数分别为13、15,质子数分别为6、7,利用质子数=电子数,质子数+中子数=质量数及同位素的概念来解答.
解答 解:A.13C与15N的中子数分别为7、8,故A错误;
B.13C、12C的中子是分别为7和6,故B错误;
C.15N与14N的质子数都是7,质子数=核电荷数,故C正确;
D.15N的核外电子数为7,中子数为15-7=8,故D错误;
故选C
点评 本题考查原子的构成及原子中的数量关系,较简单,熟悉同位素、同素异形体的概念及判断可解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.采用控制变量法设计实验方案,以2min内收集到的氧气体积作为判断依据,具体如下表所示:
(1)除上述判断反应后快慢的依据外,请另给出一种判断依据:产生气泡的快慢.
(2)探究H2O2分解快慢受浓度的影响,其实验序号分别是①>③
(3)为继续探究是CuCl2中的Cu2+对H2O2分解具有催化作用,在实验④其它条件不变的情况下,用CuSO4代替CuCl2固体进行实验,即可得出正确结论.
| 实验序号 | 温度/℃ | H2O2溶液体积及浓度 | 催化剂 | O2体积/mL(均收集2min) |
| ① | 20 | 5mL、12% | 无 | V1 |
| ② | 60 | 5mL、12% | 无 | V2 |
| ③ | 20 | 5mL、4% | 无 | V3 |
| ④ | 20 | 5mL、12% | 0.5gCuCl2固体 | V4 |
(2)探究H2O2分解快慢受浓度的影响,其实验序号分别是①>③
(3)为继续探究是CuCl2中的Cu2+对H2O2分解具有催化作用,在实验④其它条件不变的情况下,用CuSO4代替CuCl2固体进行实验,即可得出正确结论.
3.下列变化一定属于化学变化的是( )
| A. | 海水晒盐 | B. | “可燃冰”燃烧 | C. | 浓盐酸挥发 | D. | 气球爆炸 |
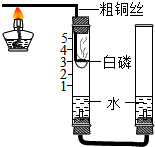 某化学兴趣小组的同学按如图装置测定空气中氧气的体积分数
某化学兴趣小组的同学按如图装置测定空气中氧气的体积分数