题目内容
3.关于Fe+2FeCl3═3X反应叙述合理的是( )| A. | 该反应涉及的物质都是由原子构成的 | |
| B. | FeCl3中铁元素、氯元素的质量比为1:3 | |
| C. | X的化学式为FeCl2 | |
| D. | Fe中铁元素的化合价为+3 |
分析 A、根据物质的构成进行分析;
B、根据化学式的有关计算进行分析;
C、根据质量守恒定律分析;
D、根据单质中元素的化合价为0分析.
解答 解:A、氯化铁是由离子构成的化合物,故错误;
B、FeCl3中铁元素、氯元素的质量比为56:(35.5×3)≠1:3,故错误;
C、根据质量守恒定律和化学方程式可知,X的化学式是FeCl2,故正确;
D、根据单质中元素的化合价为0,所以Fe中铁元素的化合价为0,故错误.
故选C.
点评 本题难度不大,掌握物质的构成、化学式的计算、质量守恒定律以及化合价的原则等即可正确解答此类题.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
13.现有一不纯的氧化铜样品16g可能混有氧化铁、氧化镁、木炭粉、氯化钠中的一种或几种,加入200g稀硫酸恰好完全反应,没有固体剩余,生成3.6g水,则下列判断正确的是( )
| A. | 原固体样品中肯定含有木炭粉 | |
| B. | 原固体样品中只混有氧化镁 | |
| C. | 恰好完全反应后溶液中水的质量为184克 | |
| D. | 所用的稀硫酸中溶质质量分数为19.6% |
14.锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示,下列说法错误的是( )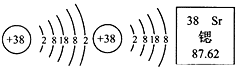

| A. | 锶的相对原子质量为87.62g | B. | 锶原子核外共有38个电子 | ||
| C. | 锶元素属于金属元素 | D. | 硫酸锶的化学式可表示为SrSO4 |
11.关于水的电解实验,下列说法正确的是( )
| A. | 这个实验证明了水是由氧气和氢气组成的 | |
| B. | 水电解是化学变化 | |
| C. | 在水通直流电后,在阳极产生体积较大的气体 | |
| D. | 实验证明水是一种混合物 |


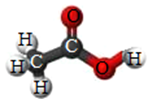 如图为某分子的结构模型,请回答下列问题:
如图为某分子的结构模型,请回答下列问题: