题目内容
9. 现有银、铜、铁三种金属,某研究小组的同学为了探究银、铜、铁的金属活动性顺序,设计了三个实验:
现有银、铜、铁三种金属,某研究小组的同学为了探究银、铜、铁的金属活动性顺序,设计了三个实验:Ⅰ.将铁片浸入稀硫酸中;Ⅱ.将银片浸入稀硫酸中;Ⅲ.将铁片浸入硫酸铜溶液中.
(1)实验Ⅲ的现象是:铁的表面有红色固体析出,溶液由蓝色变为浅绿色;写出实验Ⅰ中发生反应的化学方程式:Fe+H2SO4=FeSO4+H2↑.
(2)实验Ⅱ中没有发生化学反应,它们之间不能反应的原因是金属活动顺序表中银排在氢的后面.
(3)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的:将铜丝浸入硝酸银的溶液中,铜的表面有银白色固体析出,溶液由无色变为蓝色(写出实验操作和现象)
(4)将银、铜、铁中的两种金属分别放入硫酸铜溶液中,即可验证这三种金属的活动性强弱.
分析 (1)根据铁与稀硫酸反应,写出反应的方程式;
(2)据金属活动顺序表解答;
(3)分析上述三个实验,还不能比较铜和银活泼性,所以只要设计的实验能比较出二者的活泼性就行;
(4)根据金属与盐反应的条件考虑
解答 解:(1)将铁片浸入硫酸铜溶液中铁的表面有红色固体析出,溶液由蓝色变为浅绿色,说明铁比铜活泼;铁与稀硫酸反应,生成了硫酸亚铁和氢气,反应的方程式是:Fe+H2SO4=FeSO4+H2↑;
(2)由金属活动顺序表知银排在氢的后面,故实验Ⅱ中没有发生化学反应;
(3)将铁片浸入稀硫酸中能产生氢气,说明铁排在氢的前面,将银片浸入稀硫酸中,不反应说明银排在氢的后面;将铁片浸入硫酸铜溶液中铁的表面有红色固体析出,说明铁比铜活泼,但铜和银不能比较,所以将铜丝浸入硝酸银的溶液中,铜的表面有银白色固体析出,溶液由无色变为蓝色,说明铜比银活泼;
(4)金属与盐反应说明金属排在盐中金属的前面,金属与盐不反应,说明金属排在了盐中金属的后面,所以加入的盐溶液应该位于两种金属之间;由于铜在中间,所以两种金属放到硫酸铜溶液中即可;
答案:
(1)铁的表面有红色固体析出,溶液由蓝色变为浅绿色、Fe+H2SO4=FeSO4+H2↑;(2)金属活动顺序表中银排在氢的后面;(3)将铜丝浸入硝酸银的溶液中,铜的表面有银白色固体析出,溶液由无色变为蓝色;(4)硫酸铜.
点评 在书写铁与硫酸反应的方程式时,尤其要注意的是铁与硫酸反应生成硫酸亚铁,这是经常出现的错误.

练习册系列答案
相关题目
20.大气中存在大量的臭氧分子,其化学式是03,其中氧元素的化合价是( )
| A. | 0 | B. | +3 | C. | +2 | D. | -2 |
17.下列变化中,没有发生化学变化的是( )
| A. | 食物腐烂 | B. | 纸张燃烧 | C. | 火药爆炸 | D. | 海水晒盐 |
14.在学习碳酸钠的性质的课堂上,老师在碳酸钠溶液中加入一定量的澄清石灰水产生白色沉淀,对滤出沉淀后的滤液,引导同学们对滤液中溶质的成分进行探究.同学们通过讨论认为滤液溶质可能情况有三种:①NaOH;②NaOH和Na2CO3;③NaOH和Ca(OH)2.
小伟同学设计了下列实验方案,请你帮助完成.
小伟同学设计了下列实验方案,请你帮助完成.
| 实验步骤 | 可能出现的实验现象 | 实验结论 |
| (1)取少量滤液于试管中,加入Na2CO3溶液 | 产生白色沉淀 | 假设③成立 |
| (2)取少量的滤液于两支试管中分别加入碳酸钠溶液、稀盐酸 | 都无明显现象 | 假设①成立 |
1.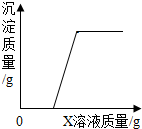 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
 向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )
向稀盐酸和硫酸铜的混合溶液中逐滴滴入X溶液至过量,生成沉淀的质量随滴入溶液质量的变化关系如图所示.则X可能是( )| A. | 硝酸银溶液 | B. | 氯化钡溶液 | C. | 硝酸钾溶液 | D. | 氢氧化钠溶液 |
18.“碱石灰”是指CaO和NaOH固体的混合物,它在空气久置会变质.某实验小组为探究一瓶久置的碱石灰样品的成分,设计了如图所示实验流程,请你参与探究过程:
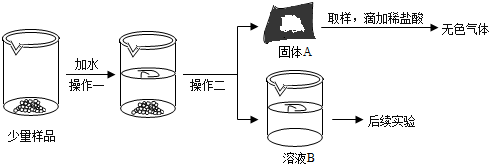
(1)使碱石灰样品充分溶解后再进行操作二,操作二的名称是过滤.
(2)根据实验现象判断固体A中一定含有碳酸钙(CaCO3).
(3)溶液B溶质的探究.
[查阅资料]①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性
[猜想]溶液B中溶质可能为:①NaOH、②Na2CO3、③NaOH和Na2CO3、④Ca(OH)2和NaOH.
[设计方案并进行实验]为了探究哪个猜想正确,同学们设计如下方案步骤并进行实验:
Ⅰ、取少量溶液B于试管中,向其中碳酸钠溶液,溶液不浑浊,证明猜想④不成立.
Ⅱ、另取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,有同学认为溶液B中的溶质一定含有NaOH,但是立即有同学反对,他的理由是碳酸钠溶液呈碱性,也能使无色的酚酞试液变成红色.
为进一步确认溶液B中溶质的成分,他做了如下实验,请填写实验报告:

(1)使碱石灰样品充分溶解后再进行操作二,操作二的名称是过滤.
(2)根据实验现象判断固体A中一定含有碳酸钙(CaCO3).
(3)溶液B溶质的探究.
[查阅资料]①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性
[猜想]溶液B中溶质可能为:①NaOH、②Na2CO3、③NaOH和Na2CO3、④Ca(OH)2和NaOH.
[设计方案并进行实验]为了探究哪个猜想正确,同学们设计如下方案步骤并进行实验:
Ⅰ、取少量溶液B于试管中,向其中碳酸钠溶液,溶液不浑浊,证明猜想④不成立.
Ⅱ、另取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,有同学认为溶液B中的溶质一定含有NaOH,但是立即有同学反对,他的理由是碳酸钠溶液呈碱性,也能使无色的酚酞试液变成红色.
为进一步确认溶液B中溶质的成分,他做了如下实验,请填写实验报告:
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
检验溶液B中溶质的存在 | ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | ①有白色沉淀生成 ②溶液由无色变为红色 | 猜想③ 正确 |
19.以下物品所用材料中,属于有机合成材料的是( )
| A. | 电脑塑料外壳 | B. | 真丝围巾 | C. | 不锈钢防盜门 | D. | 玻璃茶杯 |