题目内容
17. 实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.【查阅资料】稀盐酸能与AgNO3溶液发生复分解反应,AgCl为白色且难溶于水.
【猜想与假设】
小军的假设:澄清石灰水已变质.
小琳的假设:气体X中除了有CO2外,还有HCl气体.
【实验探究】
(1)小军的探究:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用澄清石灰水是否变质 | ①用一支试管另取少 量原澄清石灰水 ②取稀硫酸与碳酸钠 反应制取CO2 ③将生成的气体通入原澄清石灰水 | 步骤③中现象为: 石灰水不变浑浊 | 步骤②中反应方程式为: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 实验结论:所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究小琳的假设是否成立 | 将气体X通入AgNO3溶液 | 出现白色沉淀(或变浑浊) | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:小琳的假设成立 |
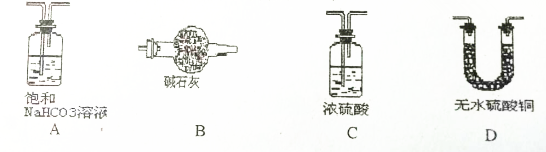
(3)同学们经过讨论发现,用如图实验装置就可以同时完成上述两个假设的探究.A、B中都盛有AgNO3溶液,通X气体后,如果A浑浊、B澄清,C浑浊,结论是小琳的假设成立(或气体中除了有CO2外,还有HCl),如果看到A浑浊、B澄清、C澄清现象,小军和小琳的结论都是正确的.
分析 【猜想与假设】
从盐酸易挥发分析;
[实验探究]I、选用其他药品制取二氧化碳,并通入原有的石灰水中,观察现象,得出结论;
II、探究气体X中是否含有氯化氢,观察现象写出结论;
[实验反思]III、根据检验气体的存在要遵循长管进,短管出的原则判断;
Ⅳ、检验Cl-是AgNO3溶液.
解答 解:
【猜想与假设】盐酸易挥发,导致气体X中除了有CO2外,还可能含有氯化氢;
[实验探究]
(1)要验证小军的假设应该把二氧化碳气体通入澄清的石灰水中,观察石灰水是否变浑浊,若变浑浊,说明石灰水没变质,反之则变质;然后写出稀硫酸与碳酸钠反应制取CO2的化学反应式和结论.
(2)探究气体X中是否含有氯化氢或HCl,将气体X通入硝酸银溶液,看硝酸银溶液是否变浑浊,如变浑浊说明有氯化氢气体,反之则没有.
[实验反思](3)试管A中放入硝酸银能检验氯化氢气体的存在,试管B中放入硝酸银溶液则是检验氯化氢气体是否被除尽,试管C是来检验二氧化碳的.
所以:如果A浑浊、B澄清、C浑浊,可以得出X为氯化氢和二氧化碳的混合气体;若小军和小琳的假设都成立,说明石灰水已变质,而X为氯化氢和二氧化碳的混合气体,所以现象是:试管C中的石灰水不会变浑浊,试管A变浑浊,试管B不变浑浊.
故答案为:[假设]HCl;
(1)小军的探究:
| 验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用澄清石灰水是否变质 | ①用一支试管另取少 量原澄清石灰水 ②取稀硫酸与碳酸钠 反应制取CO2 ③将生成的气体通入原澄清石灰水 | 步骤③中现象为: 石灰水不变浑浊 | 步骤②中反应方程式为: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 实验结论:所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究小琳的假设是否成立 | 将气体X通入AgNO3溶液 | 出现白色沉淀(或变浑浊) | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:小琳的假设成 |
点评 本题考查了二氧化碳的制取及二氧化碳、氯化氢的检验方法,较好的围绕化学实验探究的步骤进行设计实验,解题的关键是熟练掌握盐酸的挥发性、二氧化碳和氯化氢气体的检验方法等.

练习册系列答案
相关题目
7.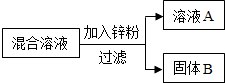 某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
【提出问题】溶液A中的溶质可能由哪些?
【作出猜想】猜想①只有Zn(NO3)2;
猜想②Zn(NO3)2、AgNO3;
猜想③Zn(NO3)2、Cu(NO3)2;
猜想④Zn(NO3)2、AgNO3、Cu(NO3)2.
【讨论交流】
若猜想③成立,则溶液A呈蓝色,固体B中一定不含的金属Zn(写化学式).四种猜想中不合理的猜想是②(填标号),其理由是猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请填写下表.
 某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.【提出问题】溶液A中的溶质可能由哪些?
【作出猜想】猜想①只有Zn(NO3)2;
猜想②Zn(NO3)2、AgNO3;
猜想③Zn(NO3)2、Cu(NO3)2;
猜想④Zn(NO3)2、AgNO3、Cu(NO3)2.
【讨论交流】
若猜想③成立,则溶液A呈蓝色,固体B中一定不含的金属Zn(写化学式).四种猜想中不合理的猜想是②(填标号),其理由是猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请填写下表.
| 实验步骤 | 现象 | 固体B的组成(写化学式) |
| 取少量固体B,滴加 稀盐酸 | 有气泡产生 | Zn、Cu、Ag |
8.小刚同学在实验室中用过氧化氢制取了氧气,实验又展开了下列思考与探究:
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
由表中数据可以得到相应的结论是二氧化锰的量会影响过氧化氢的反应速率,且在一定范围内,二氧化锰的量越大,反应速率越快.
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
由表中数据可以得到的结论是过氧化氢溶液的溶质质量分数越大,化学反应速率越快.
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量/克 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体所用时间/秒 | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..
5.鉴别下列物质的方法(括号内为方法)中不能达到目的是( )
| A. | 硬水和软水(加入肥皂水) | |
| B. | 稀HNO3和KNO3溶液(滴入酚酞试液) | |
| C. | NH4NO3和KCl固体(与熟石灰混合研磨) | |
| D. | 羊毛和涤纶(灼烧) |
2.下列各组转化中,一定条件下均能一步实现的组合是( )


| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①③ |
6.同学们填写的“毕业生登记表”需要( )
| A. | 碳素笔 | B. | 圆珠笔 | C. | 红墨水笔 | D. | 蓝墨水笔 |
7.如表是某同学用多种方法鉴别物质的情况,其中两种方法都正确的是( )
| 选项 | 需要鉴别的物质 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| A | 稀盐酸和稀硫酸 | 滴加紫色石蕊溶液 | 滴加氯化钡溶液 |
| B | 硫酸铵和磷矿粉 | 加入足量水 | 观察颜色 |
| C | 硝酸铵和硝酸钾 | 加入熟石灰、研磨 | 滴加水 |
| D | 稀烧碱溶液与石灰水 | 滴加石蕊溶液 | 加入氯化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |