题目内容
9.(1)某同学欲检验除去氨气中的水蒸气,应选择下列装置中的B,如若他想水蒸气是否完全除去,应选择下列装置中的D.(2)某兴趣小组在实验室制取二氧化碳时不小心使用了浓盐酸,制取的二氧化碳可能含有的杂质有氯化氢气体,为了得到纯净、干燥的二氧化碳,应先通入下列装置中的A,再通入C.
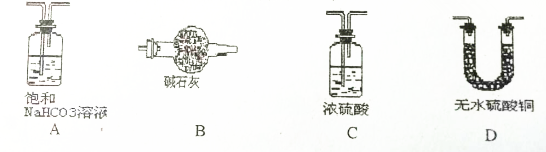
分析 (1)氨气属于碱性气体,不能用浓硫酸进行干燥,无水硫酸铜遇水变蓝;
(2)浓盐酸具有挥发性,所以制成的二氧化碳气体中混有氯化氢气体,欲除去氯化氢气体需要利用显碱性的溶液进行吸收.
解答 解:(1)氨气属于碱性气体,只能选用碱石灰进行干燥,若检验是否完全除去水蒸气,可以利用无水硫酸铜进行检验,若无水硫酸铜变蓝,则该混合气体中含有水蒸气;然后无水硫酸铜不变色,则该混合气体中不含有水蒸气.
故答案是:B;D;
(2)因为浓盐酸具有挥发性,所以利用浓盐酸制取的二氧化碳时可能含有 氯化氢气体,欲除去该气体,需要利用饱和碳酸氢钠溶液进行吸收,然后利用浓硫酸干燥酸性气体二氧化碳.
故答案是:氯化氢气体;A;C.
点评 干燥剂选择的基本原则是干燥气体时要根据干燥剂和气体的性质,选择只吸收气体中的水分,而不吸收被干燥的气体的干燥剂.即干燥剂不能和被干燥的气体发生反应.例如,不能用碱石灰、CaO和NaOH干燥CO2、SO2、HCl、H2S、Cl2、NO2等;不能用浓 H2SO4、P2O5干燥 NH3等.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
19.下列图象与对应选项关系不合理的是( )
| A. | 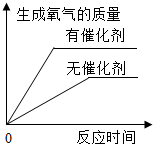 用相等质量的双氧水来制取氧气 | |
| B. | 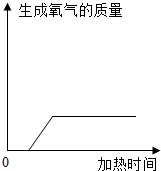 加热氯酸钾与二氧化锰的混合物制氧气 | |
| C. | 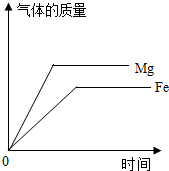 等质量的镁和铁分别与足量的同一浓度稀硫酸反应 | |
| D. | 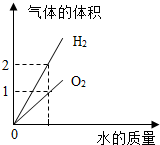 电解水生成氧气和氢气 |
20.下列关于各种气体的说法不正确的是( )
| A. | 氧气能与大多数金属反应 | B. | 氮气在空气中的质量分数约为78% | ||
| C. | 二氧化碳通入石蕊溶液能使其变红 | D. | 稀有气体通电能发出不同颜色的光 |
17. 实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
【查阅资料】稀盐酸能与AgNO3溶液发生复分解反应,AgCl为白色且难溶于水.
【猜想与假设】
小军的假设:澄清石灰水已变质.
小琳的假设:气体X中除了有CO2外,还有HCl气体.
【实验探究】
(1)小军的探究:
(2)小琳的探究
【实验反思】
(3)同学们经过讨论发现,用如图实验装置就可以同时完成上述两个假设的探究.A、B中都盛有AgNO3溶液,通X气体后,如果A浑浊、B澄清,C浑浊,结论是小琳的假设成立(或气体中除了有CO2外,还有HCl),如果看到A浑浊、B澄清、C澄清现象,小军和小琳的结论都是正确的.
 实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.
实验探究是同学们学习化学的重要部分,某学习小组用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法.【查阅资料】稀盐酸能与AgNO3溶液发生复分解反应,AgCl为白色且难溶于水.
【猜想与假设】
小军的假设:澄清石灰水已变质.
小琳的假设:气体X中除了有CO2外,还有HCl气体.
【实验探究】
(1)小军的探究:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用澄清石灰水是否变质 | ①用一支试管另取少 量原澄清石灰水 ②取稀硫酸与碳酸钠 反应制取CO2 ③将生成的气体通入原澄清石灰水 | 步骤③中现象为: 石灰水不变浑浊 | 步骤②中反应方程式为: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 实验结论:所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
| 探究小琳的假设是否成立 | 将气体X通入AgNO3溶液 | 出现白色沉淀(或变浑浊) | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:小琳的假设成立 |
(3)同学们经过讨论发现,用如图实验装置就可以同时完成上述两个假设的探究.A、B中都盛有AgNO3溶液,通X气体后,如果A浑浊、B澄清,C浑浊,结论是小琳的假设成立(或气体中除了有CO2外,还有HCl),如果看到A浑浊、B澄清、C澄清现象,小军和小琳的结论都是正确的.
14.下列各组溶液,只用一种试剂不能鉴别的是( )
| A. | FeCl2、NaNO3、Na2SO4 | B. | Na2SO4、CuSO4、NaCl | ||
| C. | (NH4)2SO4、NH4Cl、NaCl | D. | NaCl、Na2SO4、Na2CO3 |
18.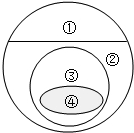 如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )
如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )
 如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )
如图所示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含于不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )| A. | ①单质 ④含氧化合物 | B. | ②化合物 ③氧化物 | ||
| C. | ①单质 ③化合物 | D. | ②化合物 ④氧化物 |
19.能源和环保是当今世界的重大问题,下列有关叙述正确的是( )
| A. | 大量使用天然气作燃料符合“低碳生活”理念 | |
| B. | 化石燃料的使用不会污染环境 | |
| C. | 风能属于“绿色能源” | |
| D. | 使用农药和化肥不会污染水 |