题目内容
13.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖.对于该溶液是否变质,同学们提出了如下假设:假设一:该溶液没有变质 假设二:该溶液全部变质 假设三:该溶液部分变质
该溶液变质的原因:CO2+2NaOH=Na2CO3+H2O(用化学方程式表示)
【查阅资料】氯化钙、氯化钠等盐溶液显中性,碳酸钠等盐溶液显碱性.
【实验验证】甲、乙两学习小组的同学找来了稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液及所需的仪器,进行实验验证.
(1)甲小组的同学所进行的实验步骤、现象及结论如下:
| 实验步骤 | 实验现象 | 结论 |
| ①取该氢氧化钠溶液样品少量于试管中,滴入过量的氯化钙溶液. | 产生白色沉淀 | 假设一不正确 |
| ②在 ①的溶液中再滴入酚酞溶液. | 溶液变红 | 假设二不正确 假设三正确 |
【实验结论】两组同学通过实验,都得出了假设三成立的结论.
【交流反思】甲组同学在实验步骤 ①中所加氯化钙溶液过量的目的是除去碳酸钠.实验步骤①中否(填:能或否)用澄清石灰水代替氯化钙溶液.
【拓展探究】
某同学决定将该部分变质的氢氧化钠溶液中的杂质除去,使它变成纯净的氢氧化钠溶液,设计的反应原理为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示),然后经过过滤实验操作得到了纯净的氢氧化钠溶液.有同学提醒不要再忘记盖瓶盖了,但发现瓶盖有玻璃塞(主要成分二氧化硅)和橡胶塞两种,你认为应当盖橡胶塞.
分析 根据氢氧化钠能与二氧化碳反应生成碳酸钠和水,检验变质就是检验碳酸钠的存在,检验变质的程度就是检验氢氧化钠的存在,结合物质间反应的实验现象进行分析解答即可.
解答 解:二氧化碳能与氢氧化钠反应生成碳酸钠和水而变质,故填:CO2+2NaOH=Na2CO3+H2O;
【实验验证】(1)加入氯化钙溶液,猜想一不成立,说明产生了白色沉淀,加入酚酞试液变红,说明含有氢氧化钠,从而证明猜想二不成立,猜想三成立,故填
| 实验步骤 | 实验现象 | 结论 |
| ①取该氢氧化钠溶液样品少量于试管中,滴入过量的氯化钙溶液. | 产生白色沉淀 | 假设一不正确 |
| ②在 ①的溶液中再滴入 酚酞溶液. | 溶液变红 | 假设二不正确 假设三正确 |
【交流反思】氯化钙溶液过量的目的是除去碳酸钠,防止对氢氧化钠的检验造成干扰,不能用石灰水代替氯化钙溶液,因为氢氧化钙能与碳酸钠反应生成氢氧化钠,故填:除去碳酸钠,否;
【拓展探究】将该部分变质的氢氧化钠溶液中的杂质除去,使它变成纯净的氢氧化钠溶液,可以加入氢氧化钙溶液,设计的反应原理为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;然后经过过滤实验操作得到了纯净的氢氧化钠溶液.由于氢氧化钠能与玻璃成分中的二氧化硅反应,故应盖橡胶塞.故填:,Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,过滤,橡胶.
点评 本题考查了久置的NaOH固体是否变质的实验探究,学生明确实验现象与结论的关系,并注意结合物质的性质来分析固体变质的原因来解答本题.检验氢氧化钠与碳酸钠的混合物时,可先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,然后使用酚酞检验氢氧化钠.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.教室是我们学习的场所.教室中的下列物质,由合成材料制成的是( )
| A. | 木制座椅 | B. | 塑料水桶 | C. | 玻璃黑板 | D. | 铝合金门窗 |
4.在下列四项操作中,正确的是( )
| A. | 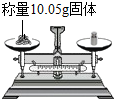 | B. | 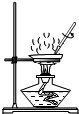 蒸发溶剂 | C. | 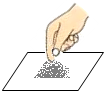 取用药品 | D. | 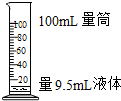 |
1.下列实验中利用提供的方案不能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明分子在不断运动 | 将一滴红墨水滴入一杯纯净水中 |
| B | 鉴别纯羊毛织品和涤纶织品 | 取样灼烧后闻气味 |
| C | 除去铁粉中混有的少量银粉 | 用足量稀盐酸溶解后过滤 |
| D | 收集二氧化碳时,检验集气瓶是否集满 | 用一根燃着的木条放在集气瓶口 |
| A. | A | B. | B | C. | C | D. | D |
8.善于归纳知识,利于培养素质.下面是某同学对部分化学知识的归纳,其中有不正确的一组是( )
| A、化学与健康 | B、实验记录 |
| ①人体缺铁会引起贫血症 ②多吃水果蔬菜利于补充维生素 ③用活性炭净水器可净化饮用水 | ①用10ml量筒量取7.25ml 水 ②用pH试纸测得苹果汁的pH为3.2 ③用托盘天平称取5.6g铁粉 |
| C、化学与能源 | D、安全常识 |
| ①煤、石油、天然气--不可再生的化石燃料 ②风能、水能、太阳能--未充分利用的绿色能源 ③使用氢能源--可以缓解温室效应,减少酸雨 | ①厨房煤气管漏气--关闭阀门并开窗通风 ②实验时碰倒酒精灯着火--用湿抹布盖灭 ③冬天用煤炉取暖--保证室内通风 |
| A. | A | B. | B | C. | C | D. | D |
18.“创建全国文明城市”,下列行为不符合这一主题的是( )
| A. | 分类回收垃圾 | B. | 禁止在公共场所吸烟 | ||
| C. | 随意燃放鞭炮 | D. | 绿色低碳出行 |
5.二氧化钛(TiO2)可制作用于家装的白色涂料,其中Ti的化合价是( )
| A. | -4 | B. | -2 | C. | +2 | D. | +4 |
2.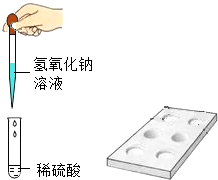 九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.
九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.
【提出问题】这些同学试管中的“氢氧化钠与稀硫酸是否恰好完全反应”?
【猜想与假设】
A.恰好完全反应 B.硫酸过量 C.氢氧化钠过量
【实验探究】
甲、乙、丙、丁四名同学分别取四个不同样品于试管中,继续探究.
(1)甲同学实验中产生蓝色沉淀的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4;
(2)请你评价乙同学的实验结论不合理,硫酸钠能与氯化钡反应产生白色沉淀;
(3)丙同学实验时观察到的现象是产生气泡(写完整).
(4)大家一致认为丁同学的实验结论错误,他能得出的结论是:反应后的溶液可能呈酸性或是中性;
【反思与收获】
(5)若要证明一个化学反应是恰好完全反应的,应设计实验证明反应物是否剩余;
【拓展延伸】
(6)溶液之间的反应可以根据需要选择“烧杯、试管、点滴板”等作为反应容器,三者比较,点滴板的优点是节约药品(写一点).
 九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.
九年一班的同学们正在分组进行“氢氧化钠溶液与稀硫酸反应”的探究实验,小组交流时大家发现有一些同学是按照如图进行的实验.【提出问题】这些同学试管中的“氢氧化钠与稀硫酸是否恰好完全反应”?
【猜想与假设】
A.恰好完全反应 B.硫酸过量 C.氢氧化钠过量
【实验探究】
甲、乙、丙、丁四名同学分别取四个不同样品于试管中,继续探究.
| 所用试剂 | 实验现象 | 实验结论 | |
| 甲同学 | 硫酸铜瘠液 | 产生蓝色沉淀 | 氢氧化钠过量 |
| 乙同学 | 氯化钡溶液 | 产生白色沉淀 | 硫酸过量 |
| 丙同学 | 锌粒 | 产生气泡 | 硫酸过量 |
| 丁同学 | 无色酚酞溶液 | 溶液不变色 | 恰好完全反应 |
(2)请你评价乙同学的实验结论不合理,硫酸钠能与氯化钡反应产生白色沉淀;
(3)丙同学实验时观察到的现象是产生气泡(写完整).
(4)大家一致认为丁同学的实验结论错误,他能得出的结论是:反应后的溶液可能呈酸性或是中性;
【反思与收获】
(5)若要证明一个化学反应是恰好完全反应的,应设计实验证明反应物是否剩余;
【拓展延伸】
(6)溶液之间的反应可以根据需要选择“烧杯、试管、点滴板”等作为反应容器,三者比较,点滴板的优点是节约药品(写一点).