题目内容
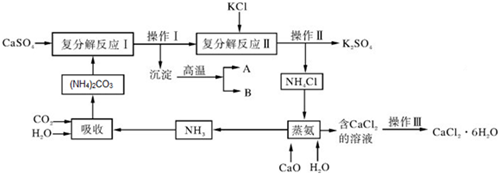
17.如图是元素周期表的一部分,据此回答下列问题.
(1)表中13号元素的原子在化学反应中易失去(填“得到”或“失去”)电子,形成离子,该元素对应的碱性物质氢氧化钠能与胃酸发生中和反应,治疗胃酸过多,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O.
(2)表中17号元素与第二周期中氟元素的化学性质相似,原因是元素的化学性质跟它的原子的最外层电子数目关系非常密切;
(3)表中12号元素与16号元素的单质中加热时反应的化学方程式为Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS,该反应的基本反应类型是化合反应.
分析 (1)13号元素的原子最外层电子数为3,结合若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;氢氧化铝与胃酸中的盐酸反应生成氯化铝和水,写出反应的化学方程式即可.
(2)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
(3)根据元素周期表分析12号元素和16号元素的单质名称,然后写出反应方程式.
解答 解:(1)13号元素的原子最外层电子数为3,在化学反应中易失去3个电子而形成带3个单位正电荷的阳离子.
氢氧化铝与胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
故填:失去;Al(OH)3+3HCl═AlCl3+3H2O;
(2)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,17号元素的最外层电子数为7,与第二周期中的氟元素的化学性质相似.故填:氟;元素的化学性质跟它的原子的最外层电子数目关系非常密切;
(3)从元素周期表可以知道12号元素的单质是镁、16号元素的单质是硫,镁和硫在加热的条件下化合的化学方程式:Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS;该反应是两种物质生成一种物质的反应,是化合反应;故答案为:Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS;化合反应.
点评 本题难度不大,掌握元素周期表的含义、原子结构示意图的含义、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
5.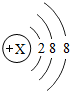 某粒子结构示意图如图所示,下列对该粒子的说法中,不正确的是( )
某粒子结构示意图如图所示,下列对该粒子的说法中,不正确的是( )
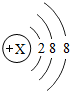 某粒子结构示意图如图所示,下列对该粒子的说法中,不正确的是( )
某粒子结构示意图如图所示,下列对该粒子的说法中,不正确的是( )| A. | 该粒子核内质子数X=18 | |
| B. | 该粒子的核外电子是分层排布的 | |
| C. | 该粒子具有相对稳定的结构 | |
| D. | 该粒子可能是阳离子或阴离子或稀有气体原子 |
12.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | K2CO3 HCl Na2SO4 | B. | KNO3 HCl NaCl | ||
| C. | H2SO4 FeCl3 KOH | D. | CuSO4 HCl NaNO3 |
9.下列方案合理的是( )
| A. | 测一木块长度时,为减小误差可多次测量取平均值 | |
| B. | 检验碳酸根离子:将要检验的物质与稀盐酸混合,观察是否产生气泡 | |
| C. | 验证质量守恒定律:将锌粒与细流散混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
6.某固体物质受热后变为气态物质,这种变化属于( )
| A. | 化学变化 | |
| B. | 可能是物理变化,也可能是化学变化 | |
| C. | 物理变化 | |
| D. | 既不是物理变化,也不是化学变化 |
7.下列变化中属于化学变化的是( )
| A. | 西瓜榨汁 | B. | 粉碎废纸 | C. | 燃放烟花 | D. | 滴水成冰 |