题目内容
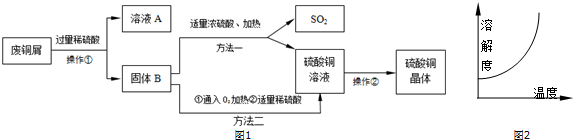
8.在工业上可以用纯碱和石灰石为原料制备烧碱,主要流程如图所示:
(1)在①-④四个过程中,发生了化合反应的为②(填序号).
(2)③中实验操作过程的名称为溶解,经搅拌后,得到石灰水.
(3)NaCl、KNO3、Ca(OH)2三物质的溶解度曲线图分别如图一、图二所示,请回答:

①由图一可知,20℃时 KNO3溶液的溶质质量分数无法确定NaCl 溶液的溶质质量分数 (填“大于”“小于”“等于”“无法确定”之一).
②由图一可知,将 20℃时 KNO3饱和溶液升温到 50℃时,溶液的溶质质量分数不变(填“变大”“变小”“不变”之一).
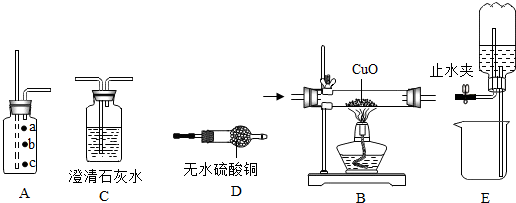
③如图三所示,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体,结合图二分析石灰水中可出现浑浊的现象.
分析 (1)高温条件下,碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
(2)③中实验操作过程的名称为溶解,经搅拌后,得到石灰水;
(3)溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
氢氧化钠溶于水放出热量.
解答 解:(1)高温条件下,碳酸钙分解生成氧化钙和二氧化碳,属于分解反应;
氧化钙和水反应生成氢氧化钙,属于化合反应;
氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,属于复分解反应.
故填:②.
(2)③中实验操作过程的名称为溶解,经搅拌后,得到石灰水.
故填:溶解.
(3)①因为不知道溶液是否饱和,因此无法比较20℃时KNO3溶液的溶质质量分数和NaCl 溶液的溶质质量分数大小.
故填:无法确定.
②由图一可知,硝酸钾的溶解度随着温度升高而增大,将20℃时KNO3饱和溶液升温到50℃时,溶液变成不饱和溶液,溶质质量和溶液质量都不变,因此溶液的溶质质量分数不变.
故填:不变.
③如图三所示,氢氧化钙的溶解度随着温度升高而减小,20℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体,溶液温度升高,氢氧化钙溶解度减小,一部分氢氧化钙从溶液中析出,溶液变浑浊.
故填:浑浊.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
13.在人体上发生的下列变化中,属于化学变化的是( )
| A. | 皮肤破损 | B. | 骨折 | C. | 消化食物 | D. | 切除肿瘤 |
20.在水蒸发变成水蒸气的过程中,物质的体积增大的原因是( )
| A. | 水分子之间间隔增大 | B. | 水分子个数增多 | ||
| C. | 水分子分成更小的微粒 | D. | 水分子体积增大 |