题目内容
12.已知镁能在氮气中燃烧,生成氮化镁(氮元素-3价).氮化镁是一种灰绿色固体,极易与水反应生成白色沉淀Y(一种碱),并放出能使湿润的红色石蕊试纸变蓝色的气体R,反应的方程式可表示为:X(氮化镁)+6H2O═mY↓+nR↑.请回答下列问题:(1)氮化镁的化学式为Mg3N2,其中镁与氮元素的质量比为7:18.(最简整数比)
(2)上述反应方程中,“mY、nR”分别是3Mg(OH)2、2NH3.
(3)若24g镁在空气中完全燃烧,生成含镁元素固体的质量<(填>、=、<)40g.
分析 (1)根据元素化合价进行分析解答.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据质量守恒定律来分析解答;
(3)假定产物全部是氧化镁或氮化镁,所得产物的质量应介于二者之间.可采用极端假设法来解答本题.
解答 解:(1)根据氮化镁中镁元素是+2价,氮元素-3价.故氮化镁的化学式是Mg3N2,进行计算:氮化镁中氮元素与镁元素的质量比为(14×2):(24×3)=7:18.
(2)氮化镁是一种灰绿色固体,极易与水反应生成白色沉淀Y(一种碱),并放出能使湿润的红色石蕊试纸变蓝色的气体R;故Y即为氢氧化镁,R为氨气;故化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
(3)设若产物全部为氧化镁时产物的质量为x.
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO
48 80
24g x
则$\frac{48}{24g}=\frac{80}{x}$,解得x=40g
设若产物全部为氮化镁时产物的质量为y.
3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
72 100
24g y
则$\frac{72}{24g}=\frac{100}{y}$,解得y=33.3g
通过以上计算可知所得产物质量应在33.3g与40g之间.
故答案为:
(1)Mg3N2.7:18.(2)3Mg(OH)2;2NH3.(3)<.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.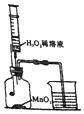 如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2.
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是燃烧匙中白磷不燃烧是因为未达到白磷的着火点;水中白磷不燃烧是因为没有与氧气接触;推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧.
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,该实验中,集气瓶内压强的变化过程是先增大后减小.
 如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O.
如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃,2NaOH+CO2═Na2CO3+H2O. | 内容步骤 | [实验1]研究燃烧条件 | [实验2]研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是燃烧匙中白磷不燃烧是因为未达到白磷的着火点;水中白磷不燃烧是因为没有与氧气接触;推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧.
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是支持燃烧;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,该实验中,集气瓶内压强的变化过程是先增大后减小.
20.化学科学为人类文明和社会进步作出了巨大贡献,下列认识中错误的是( )
| A. | 化学科学的发展为人类研制新材料提供了保证 | |
| B. | 我国歼20飞机、神舟飞船和航空母舰等装备的研制与化学科学无关 | |
| C. | 化学工业是把双刃剑,在提升人们生活品质的同时,也可能会造成环境污染 | |
| D. | 开发利用氢能、太阳能和潮汐能,符合低碳生活理念 |
7.下列是初中化学常用的一些实验仪器: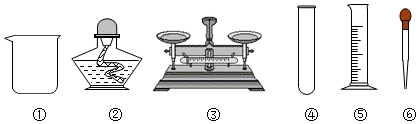
若用固体氯化钠配制50g溶质质量分数为12%的氯化钠溶液,在配制过程中需要用到的仪器组合是( )

若用固体氯化钠配制50g溶质质量分数为12%的氯化钠溶液,在配制过程中需要用到的仪器组合是( )
| A. | ①②③⑤ | B. | ①③⑤⑥ | C. | ①②③④ | D. | ③⑤⑥ |
4.环境空气质量标准增加了PM2.5监测指标.PM2.5是指大气中直径小于或等于2.5μm的可吸入颗粒物.下列能减少PM2.5污染的一项是( )
| A. | 积极植树造林 | B. | 露天焚烧垃圾 | C. | 排放汽车尾气 | D. | 用煤作燃料 |
1.下列利用了乳化原理的是( )
| A. | 用洗洁精除去餐具上的油污 | B. | 用稀硫酸除铁锈 | ||
| C. | 用汽油除去衣服上的油污 | D. | 用食醋除去水垢 |
2.车用乙醇汽油是由乙醇与汽油按1:9的比例混合而成,下列有关推广使用乙醇汽油的说法不正确的是( )
| A. | 可以节约化石燃料 | |
| B. | 有助于减轻大气污染,改善大气环境 | |
| C. | 乙醇是一种不可再生的能源 | |
| D. | 有助于促进粮食转化,提高农民收入 |
