题目内容
17.实验室用氯酸钾和二氧化锰的混合物制取氧气,某次实验中固体的质量变化如下: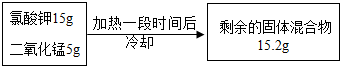
(1)生成氧气的物质的量为0.15mol.
(2)求参加反应的氯酸钾的物质的量.(根据化学方程式列式计算)
(3)根据题目中所给条件,判断氯酸钾是否已经完全分解?否(填“是”或“否”).
分析 根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,依据质量守恒定律计算出氧气的质量,再结合方程式计算题中的其他数据.
解答 解:(1)根据质量守恒定律可知,生成氧气的质量为:15g+5g-15.2g=4.8g,所以氧气的物质的量:$\frac{4.8g}{32g/mol}$=0.15mol;故填:0.15;
(2)设参加反应的氯酸钾的物质的量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
2 3
x 0.15mol
$\frac{2}{x}=\frac{3}{0.15mol}$
x=0.1mol
答:参加反应的氯酸钾的物质的量为0.1mol.
(3)参加反应氯酸钾的质量=0.1mol×122.5g/mol=12.25g,原有氯酸钾的质量为15g,所以根据题目中所给条件,可知氯酸钾没有完全分解.故填:否.
点评 本题主要考查学生对物质质量守恒定律的认识以及利用化学方程式进行计算的能力,解题的关键是利用质量守恒定律求出氧气的质量.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
7.下列生活中常见的变化,属于化学变化的是( )
| A. | 石烛熔化 | B. | 铁生锈 | C. | 玻璃破碎 | D. | 汽油挥发 |
8.下列变化过程中一定会发生化学变化的是( )
| A. | 物质由固态变成气态 | B. | 向澄清的石灰水中吹气 | ||
| C. | 工业上制取氧气 | D. | 把黄瓜切成细丝 |
5.下列有关实验现象的描述中,错误的是( )
| A. | 纯净的氢气能在空气中安静地燃烧,产生淡蓝色火焰 | |
| B. | 给碱式碳酸铜加热时,能看到黑色固体逐渐变为绿色 | |
| C. | 镁条在空气中燃烧,发出耀眼的白光,生成白色固体,放出热量 | |
| D. | 木炭在氧气中燃烧,发出白光,产生的气体能使澄清石灰水变浑浊 |
12.某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g晶体,再恒温蒸发掉10g水,析出了3g晶体,则下列说法正确的是( )
| A. | 此物质在t℃时的溶解度为$\frac{30g}{100g}$水 | |
| B. | 最后剩余溶液是不饱和溶液 | |
| C. | 最后剩余的溶液一定比原溶液稀 | |
| D. | 原溶液在t℃时一定是饱和溶液 |
2.下列实验操作中正确的是( )
| A. |  倾倒液体 | B. | 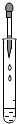 滴加液体 | C. | 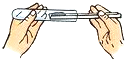 向试管中装固体 | D. | 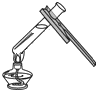 加热液体 |
9.下列关于电解水的实验叙述正确的是( )
| A. | 正极产生的是氧气,具有可燃性 | |
| B. | 实验开始前,两量气管内不必充满水 | |
| C. | 该实验说明水是由氢气和氧气组成的 | |
| D. | 负极和正极气体的体积比约为2:1 |
6.如图是某品牌500毫升装矿泉水标签的一部分,回答相关问题
(1)表中的钠、镁、钾、钙都是指元素.(选填“分子”、“原子”或“元素”)
(2)喝一瓶该矿泉水,最多摄入的偏硅酸的质量为35mg.
(3)生产矿泉水时,对于水中的不溶性固体,可以通过过滤的方法去除.
(4)可以使用肥皂水检验该矿泉水是不是硬水;生活中通常使用煮沸的方法降低水的硬度,在煮沸过程中,溶解在水中的碳酸氢钙会分解成一种白色沉淀、水和二氧化碳,请写出该反应的文字表达式碳酸氢钙$\stackrel{加热}{→}$碳酸钙+水+二氧化碳.
天然矿物质含量:mg/L
(1)表中的钠、镁、钾、钙都是指元素.(选填“分子”、“原子”或“元素”)
(2)喝一瓶该矿泉水,最多摄入的偏硅酸的质量为35mg.
(3)生产矿泉水时,对于水中的不溶性固体,可以通过过滤的方法去除.
(4)可以使用肥皂水检验该矿泉水是不是硬水;生活中通常使用煮沸的方法降低水的硬度,在煮沸过程中,溶解在水中的碳酸氢钙会分解成一种白色沉淀、水和二氧化碳,请写出该反应的文字表达式碳酸氢钙$\stackrel{加热}{→}$碳酸钙+水+二氧化碳.
天然矿物质含量:mg/L
| 偏硅酸 | 25.0~70.0 |
| 钠 | 1.0~25.0 |
| 镁 | 0.1~15.0 |
| 钾 | 0.5~10.0 |
| 钙 | 2.0~35.0 |
| 溶解性总固体 | 50.0~250.0 |