题目内容
6.水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答:(1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏.
(2)硬水给生活和生产带来很多麻烦,生活中可用肥皂水来区分硬水和软水,常用加热煮沸或蒸馏的方法来降低水的硬度.
(3)地球上的总储水量虽然很大,但淡水很少,爱护水资源是每个公民的责任和义务.下列行为属于节约用水的是B(填序号)
A.公共场所不用随手关水龙头 B.洗完菜的水用来浇花 C.不间断放水刷牙.
分析 (1)根据已有的知识进行分析,蒸馏获得的水是纯净水;
(2)鉴别硬水和软水使用肥皂水;加热煮沸或蒸馏能降低水的硬度;
(3)根据节约用水的方法进行分析解答.
解答 解:(1)蒸馏获得的水是纯净水,是净化程度最高的净水方法,故填:蒸馏;
(2)鉴别硬水和软水使用肥皂水,与肥皂水混合产生浮渣的是硬水,与肥皂水混合产生泡沫的是软水;降低水的硬度就是减少水中可溶性钙镁化合物的含量,可以采用加热煮沸或蒸馏的方法,故填:肥皂水;煮沸(或蒸馏);
(3)A、公共场所不用随手关水龙头,这是浪费水的做法,不可取,
B、洗完菜的水用来浇花,这种做法能提高水的利用率,可节约用水,
C、不间断放水刷牙,这会浪费水,故选B.
故答案是:(1)蒸馏;
(2)肥皂水、加热煮沸或蒸馏;
(3)B.
点评 本题较简单,但要熟悉净水方法,学会区分硬水和软水,还要树立节约用水的意识.

练习册系列答案
相关题目
17.化学实验小组同学在发现实验台上放置了一瓶固体和一瓶液体,是初中常见的药品,但标签已经无法辨别.他们取了少量药品混合后有气泡产生,于是想探究产生的这种气体.具体实验如下:

(1)从图中选择发生装置是B(填序号,下同);
(2)用干燥后的该气体吹肥皂泡,发现肥皂泡下沉,可以判断该气体一定不是C;
A.O2 B.CO2 C.H2
(3)欲用排空气法收集一瓶上述气体,则应该选择D装置;
(4)为了进一步确定该气体的成分,请你设计检验气体的方法并完成下表:
(5)写出产生该气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.

(1)从图中选择发生装置是B(填序号,下同);
(2)用干燥后的该气体吹肥皂泡,发现肥皂泡下沉,可以判断该气体一定不是C;
A.O2 B.CO2 C.H2
(3)欲用排空气法收集一瓶上述气体,则应该选择D装置;
(4)为了进一步确定该气体的成分,请你设计检验气体的方法并完成下表:
| 检验方法 | 现象 | 结论 |
| 用带火星的木条伸入集气瓶中 | 木条复燃 | 该气体是氧气 |
1.金属材料被广泛的应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关.下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究.
【实验目的】测定金属铁、铜和镁的活动性强弱
【实验过程】
步骤Ⅰ将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的稀硫酸的试管中;
步骤Ⅲ将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“×”表示能观察不到实验现象,用“√”表示观察到实验现象(见表).
实验现象记录表
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是在空气中,镁能和氧气反应的最剧烈
(2)记录表A处应填写的现象是是金属铜表面附着着一层银白色的金属,溶液的颜色由无色变为蓝色,该反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、浓度以外,还需要控制的条件是溶液的种类.写出镁和稀硫酸反应的化学方程式Mg+H2SO4=MgSO4+H2↑,此反应属于置换反应.
【实验结论】金属锌、铜和镁的活动性由弱到强的顺序是Mg、Fe、Cu(用元素符号表示)
【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属锌和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是Mg和H2SO4反应速度太快,不易控制.
【实验目的】测定金属铁、铜和镁的活动性强弱
【实验过程】
步骤Ⅰ将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的稀硫酸的试管中;
步骤Ⅲ将铁片、铜片、镁片分别放入三只盛有浓度相同、体积相同的硝酸银溶液的试管中.
【实验记录】用“×”表示能观察不到实验现象,用“√”表示观察到实验现象(见表).
实验现象记录表
| 金属 | 空气 | 稀硫酸 | 硝酸银 |
| 铁 | × | √ | √ |
| 铜 | × | × | √(A) |
| 镁 | √ | √ | √ |
(2)记录表A处应填写的现象是是金属铜表面附着着一层银白色的金属,溶液的颜色由无色变为蓝色,该反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、浓度以外,还需要控制的条件是溶液的种类.写出镁和稀硫酸反应的化学方程式Mg+H2SO4=MgSO4+H2↑,此反应属于置换反应.
【实验结论】金属锌、铜和镁的活动性由弱到强的顺序是Mg、Fe、Cu(用元素符号表示)
【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属锌和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是Mg和H2SO4反应速度太快,不易控制.
16.某课外活动小组为探究蜡烛的有关化学性质,已进行了查资料(内容略)、部分实验设计和观察及假设了部分结论,假如你是该组的成员
(1)请你根据如表完成整个探究报告(填写在表中)
(2)请回答在探究活动中,除经历提出问题、查资料、猜想与假设、设计实验方案阶段外,还可能经历了哪些阶段进行实验操作(或实施实验方案),观察并记录实验现象,分析并得出结论(或表达与交流得出结论).
(1)请你根据如表完成整个探究报告(填写在表中)
| 实验操作及实验作图 | 实验现象 | 结 论 |
 A.将燃烧的蜡烛用烧杯将其罩住 | 蜡烛火焰逐渐变小直至熄灭,烧杯内壁有水雾,烧杯壁有黑色颗粒 | 蜡烛燃烧需要氧气(或烧杯内氧气基本耗尽). |
 B.将一根细木条按下图所示放入火焰中,约2秒后立即取出 | 木条中间被烧痕迹最轻, 越向两侧被烧痕迹越重 | 焰心和内焰的温度低于外焰的温度(或焰心、内焰、外焰温度不同) |
 C.将涂有少量澄清石灰水的玻璃片放在火焰上方 | 玻璃片上澄清的石灰水变浑浊(或玻璃片上有一层白膜生成) | 蜡烛燃烧时生成二氧化碳气体,证明蜡烛的组成中一定含有碳元素 |
| D.假如蜡烛中含有氢元 素,那么蜡烛燃烧的产物中 有水生成.请依据此假设写 出操作步骤(不作图). | 在火焰的上方罩一个干、冷小烧杯(或在火焰的上方放一个干、冷的玻璃片) | \ |
 在实验室可用如图装置制取蒸馏水,回答下列问题
在实验室可用如图装置制取蒸馏水,回答下列问题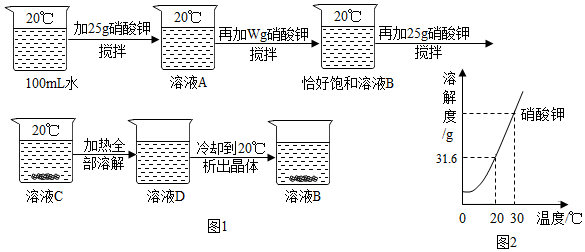
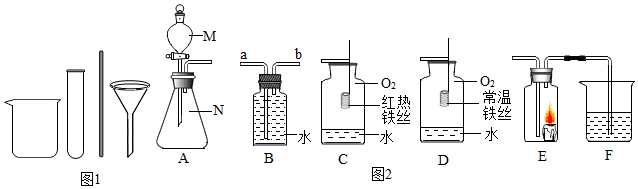
 甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应,进行总结归纳并回答下列问题:
甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应,进行总结归纳并回答下列问题: