题目内容
16.图1是A、B、C微粒的结构示意图,图2是两种元素在元素周期表中的信息.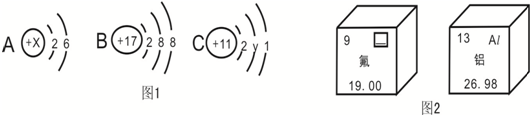
(1)图1中A结构示意图中x=8;C结构示意图中y=8;
(2)图2中方框内的横线上应填的元素符号是F;图1中B结构示意图的化学符号为Cl-.
(3)图1中B C结构示意图表示的微粒结合形成的物质的化学式为NaCl.
分析 (1)在原子中,核内质子数等于等于核外电子数;根据核外电子排布的特点,第二层排满时排8个电子;(2)由元素在周期表中的相关信息可知,方框内的横线上应填氟元素的符号,由图1中B结构示意图的可知,核内质子数是17的元素是氯元素,可以写出微粒的符号;
(3)根据它们得失电子情况,判断其组成的化合物的化学式.
解答 解:(1)在原子中,核内质子数等于等于核外电子数,图1中A结构示意图中x=8,第二层排满时排8个电子;
(2)由元素在周期表中的相关信息可知,方框内的横线上应填氟元素的符号:F,由图1中B结构示意图的可知,核内质子数是17的元素是氯元素,该微粒为氯离子,符号为:Cl-;
(3)由图1中结构示意图表示的微粒可以看出,B粒子为氯离子,C粒子为钠原子,可以失1个电子,形成的化合物的化学是为:NaCl.
故答为:(1)8;8;阴离子;(2)F,Cl-;(3)NaCl.
点评 了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点;了解元素周期表的特点及其应用.

练习册系列答案
相关题目
9.你认为下列的实验方案中可行的是( )
| A. | 把Mg、Zn、Cu、Ag分别插入同体积、同质量分数的稀盐酸中,比较四种金属的活泼性 | |
| B. | 加热水的方法测定水的组成 | |
| C. | 按溶解、过滤、蒸发的操作顺序分离Na2CO3和BaCO3 | |
| D. | 按方案:NaOH$\stackrel{+稀盐酸}{→}$NaCl$\stackrel{+KNO_{3}}{→}$NaNO3,制取Na |
4.下列属于溶液的是( )
| A. | 泥水 | B. | 植物油滴在水中 | C. | 水 | D. | 稀硫酸 |
1.下列对相关实验现象的描述错误的是( )
| A. | 在纯碱溶液中滴加紫色石蕊试液后溶液变蓝 | |
| B. | 向氯化亚铁溶液中滴加氢氧化钠溶液,生成红褐色沉淀 | |
| C. | 双氧水分解时放出热量 | |
| D. | 聚氯乙烯在空气中灼烧有刺激性气味 |
8. 燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )
燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )
 燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )
燃烧是人类最早利用的化学反应之一,但是燃烧引发的火灾也会给人类带来灾难.已知某化合物的着火点为t1,该物质易在空气中失火,则如图所示的A、B、C、D点中,表示完全可以灭火的是( )| A. | A点和D点 | B. | A点和B点 | C. | B点和C点 | D. | C点和D点 |
5.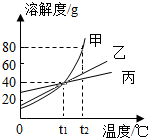 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )
 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )| A. | 甲、乙、丙三者的溶解度相同 | |
| B. | t1℃时100g甲的饱和溶液中含有40g甲 | |
| C. | t2℃时,往100 g水中加入90 g甲,充分搅拌后得到190 g甲的溶液 | |
| D. | t1℃时甲、乙、丙三者饱和溶液的溶质质量分数相等 |
6.空气成分中能参与植物光合作用的气体是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | 稀有气体 |
