题目内容
5.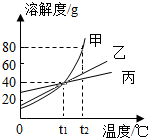 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息正确的是( )| A. | 甲、乙、丙三者的溶解度相同 | |
| B. | t1℃时100g甲的饱和溶液中含有40g甲 | |
| C. | t2℃时,往100 g水中加入90 g甲,充分搅拌后得到190 g甲的溶液 | |
| D. | t1℃时甲、乙、丙三者饱和溶液的溶质质量分数相等 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、固体物质的溶解度受温度影响较大,没有指明温度,不能比较溶解度的大小,故A错误;
B、t1℃时,甲物质的溶解度是40g,140g甲的饱和溶液中含有40g甲,故B错误;
C、t2℃时,甲物质的溶解度是80g,所以往100g水中加入90g甲,充分搅拌后得到180g甲的溶液,故C错误;
D、t1℃时甲、乙、丙三种物质的溶解度相等,所以三者饱和溶液的溶质质量分数相等,故D正确.
故选:D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
18.为减轻大气污染,可将汽车尾气中的CO和NO转化为无毒气体,转化的无毒气体可能是( )
| A. | N2和CO2 | B. | CO2和NO2 | C. | CO2 和 O2 | D. | CO2和SO2 |
13.生活中的下列物质,属于纯净物的是( )
| A. | 厨房的食用盐 | B. | 铝合金门窗 | C. | 食品袋里的氮气 | D. | 康师傅矿泉水 |
14.以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理的是( )
| 序号 | 化学反应事实 | 影响反应的因素 |
| A | 木炭在纯氧中比在空气中燃烧更剧烈 | 反应物浓度 |
| B | 水要通电才能分解,而双氧水加入二氧化锰就迅速分解 | 催化剂 |
| C | 碳在常温下不与氧气发生反应而在高温时能与氧气反应 | 反应温度 |
| D | 铜片在空气中很难燃烧,超细纳米铜粉在空气中易燃烧 | 反应物的接触面积 |
| A. | A | B. | B | C. | C | D. | D |
12.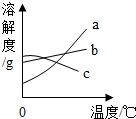 如图三条溶解度曲线,当它们的溶液接近饱和时,分别采用冷却热饱和溶液、蒸发溶剂、增加溶质的方法,均可使它变为饱和溶液的是( )
如图三条溶解度曲线,当它们的溶液接近饱和时,分别采用冷却热饱和溶液、蒸发溶剂、增加溶质的方法,均可使它变为饱和溶液的是( )
 如图三条溶解度曲线,当它们的溶液接近饱和时,分别采用冷却热饱和溶液、蒸发溶剂、增加溶质的方法,均可使它变为饱和溶液的是( )
如图三条溶解度曲线,当它们的溶液接近饱和时,分别采用冷却热饱和溶液、蒸发溶剂、增加溶质的方法,均可使它变为饱和溶液的是( )| A. | a溶液 | B. | b,c溶液 | C. | c溶液 | D. | a,b溶液 |
 在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.
在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.