题目内容
8.实验室有一瓶含有K2CO3和K2SO4的混合溶液,某化学兴趣小组设计实验来测定溶质的质量分数.他们经过讨论后设计了如下装置进行实验探究: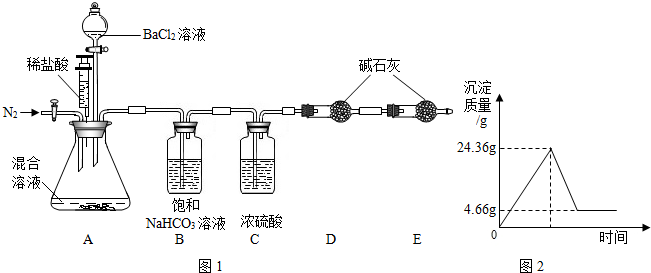
a.按图组装仪器,检查气密性,把100g混合溶液加入锥形瓶中装好药品;
b.打开A中活塞,通入N2一段时间,再关闭活塞,称得D装置的质量为m1g;
c.逐滴加入BaCl2溶液至不再产生沉淀;关闭分液漏斗,再用针筒打入稀盐酸,至不再产生气体,实验过程中测得锥形瓶中沉淀的数据如右图;
d.打开A中活塞,缓缓通一会儿N2;
e.再称得D装置的质量为m2g.
请你根据题意回答下列问题:
(1)24.36g沉淀中含有什么物质?BaCO3、BaSO4(填化学式).针筒注入稀盐酸产生气体的化学方程式为BaCO3+2HCl=BaCl2+H2O+CO2↑.
(2)求原混合液中K2SO4的质量分数.
(3)小明略加思考后说,通过D装置的质量变化可以求出混合溶液中K2CO3的质量分数,结果偏大(选填“偏大”、“不变”或“偏小”),理由是盐酸挥发出的HCl气体与B装置中NaHCO3反应,生成的CO2也一并被D装置中的碱石灰吸收了,所以CO2的质量偏大,导致算出的结果偏大.
分析 (1)根据氯化钡溶液和碳酸钾溶液反应生成碳酸钡沉淀和氯化钾,氯化钡溶液和硫酸钾溶液反应生成硫酸钡沉淀和氯化钾,盐酸和碳酸钡反应生成氯化钡、水和二氧化碳进行解答;
(2)根据硫酸钡不溶于稀盐酸,所以由图2可知4.66g沉淀就是生成的硫酸钡沉淀,利用硫酸钡的质量求出硫酸钾的质量,即可求出原混合液中K2SO4的质量分数;
(3)根据盐酸挥发出的HCl气体与B装置中NaHCO3反应,生成的CO2也一并被D装置中的碱石灰吸收了,所以CO2的质量偏大,导致算出的结果偏大进行解答.
解答 解:(1)根据氯化钡溶液和碳酸钾溶液反应生成碳酸钡沉淀和氯化钾,反应的化学方程式为:K2CO3+BaCl2=BaCO3↓+2KCl;氯化钡溶液和硫酸钾溶液反应生成硫酸钡沉淀和氯化钾,K2SO4+BaCl2=BaSO4↓+2KCl,所以24.36g沉淀中含有碳酸钡和硫酸钡;盐酸和碳酸钡反应生成氯化钡、水和二氧化碳,反应的化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑;
(2)硫酸钡不溶于稀盐酸,所以由图2可知4.66g沉淀就是生成的硫酸钡沉淀.
设硫酸钾的质量为x.
K2SO4+BaCl2=BaSO4↓+2KCl
174 233
x 4.66g
$\frac{174}{x}$=$\frac{233}{4.66g}$
x=3.48g
原混合液中K2SO4的质量分数为:$\frac{3.48g}{100g}$×100%=3.48%
答:原混合液中K2SO4的质量分数为3.48%;
(3)盐酸挥发出的HCl气体与B装置中NaHCO3反应,生成的CO2也一并被D装置中的碱石灰吸收了,所以CO2的质量偏大,导致算出的结果偏大.
故答案为:(1)BaCO3、BaSO4;BaCO3+2HCl=BaCl2+H2O+CO2↑;
(2)3.48%;
(3)偏大,盐酸挥发出的HCl气体与B装置中NaHCO3反应,生成的CO2也一并被D装置中的碱石灰吸收了,所以CO2的质量偏大,导致算出的结果偏大.
点评 实验探究题包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 溶液的质量不变 | |
| B. | 溶液中溶质的质量分数降低 | |
| C. | 溶液中硝酸钾的溶解度不变 | |
| D. | 有晶体析出,饱和溶液变为不饱和溶液 |
| A. | Fe+CuSO4═FeSO4+Cu | B. | NaOH+HCl═NaOH+H2O | ||
| C. | CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | D. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ |
| A. | A3B2 | B. | A2B3 | C. | AB2 | D. | AB3 |
| A. | CO2+2 NaOH=Na2CO3+H2O | B. | HCl+AgNO3=AgCl↓+HNO3 | ||
| C. | H2SO4+CuO=CuSO4+H2O | D. | HCl+NaOH=NaCl+H2O |
| A. | 红色 | B. | 蓝色 | C. | 紫色 | D. | 无色 |