题目内容
14.小明同学得到了如下关于A、B的两种固体物质的溶解度表:| 温度(℃) | 0 | 10 | 20 | 30 | 40 | |
| 溶解度(g) | A | 35 | 35.5 | 36 | 36.5 | 37 |
| B | 6 | 10 | 18 | 36.5 | 50 | |
(2)我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”.据此你认为表中A(填“A”或“B”)物质的溶解度与氯化钠相似.
分析 (1)根据A、B的两种固体物质的溶解度表,B的溶解度随着温度的升高而增大,溶解度受温度的影响变化较大,进行分析解答.
(2)夏天晒盐,是因为氯化钠的溶解度受温度影响变化不大,夏天温度高,水分蒸发快,氯化钠易结晶析出,进行分析解答.
解答 解:(1)由A、B的两种固体物质的溶解度表,B的溶解度随着温度的升高而增大,溶解度受温度的影响变化较大,一般采用降温结晶的方法,降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出.
(2)夏天晒盐,是因为氯化钠的溶解度受温度影响变化不大,夏天温度高,水分蒸发快,氯化钠易结晶析出,表中A的溶解度受温度影响变化不大,A物质的溶解度与氯化钠相似.
故答案为:(1)降温结晶;(2)A.
点评 本题难度不大,掌握降温结晶和蒸发结晶的原理并能灵活运用是正确解答本题的关键.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
4.小岳同学在复习气体的性质时,阅读到以下资料:制取气体的发生装置取决于反应前的药品状态和反应条件,收集气体的装置取决于气体能否与水反应、在水中的溶解性以及该气体相对于空气的密度大小.现有甲、乙、丙三种气体的反应前的物品状态、反应条件以及有关性质如下表,有关装置如下图.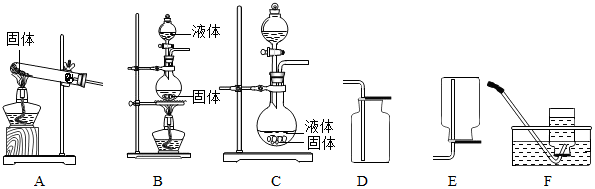
请你回答下列问题:
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)收集乙气体应选择的装置是E(填字母序号);
(3)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.

| 气体 | 反应前的药品状态 | 反应条件 | 气体性质 |
| 甲 | 固体+液体 | 常温 | 不与水反应,不易溶于水,密度比空气大 |
| 乙 | 固体+固体 | 加热 | 能与水发生反应,易溶于水,密度比空气小 |
| 丙 | 固体+液体 | 加热 | 能与水发生反应,能溶于水,密度比空气大 |
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)收集乙气体应选择的装置是E(填字母序号);
(3)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
5.下列各组物质的名称、俗称和化学式表示同一种物质的是( )
| A. | 氧化铁、铁锈、Fe3O4 | B. | 氢氧化钙、消石灰、Ca(OH)2 | ||
| C. | 纯碱、烧碱、Na2CO3 | D. | 碳酸钙、熟石灰、CaCO3 |
9.根据下表问题.
(1)60℃时,向两个分别盛有50g氯化钠和氯化铵的烧杯中,各加入100g的水.充分溶解后,达到饱和的是NaCl溶液.
(2)采用一种操作方法,将上述另一种未饱和的溶液变为饱和,下列说法正确的是CD(填字母序号,可多选).
A.溶液中溶质的质量一定增加 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可降低温度或增加溶质.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
(2)采用一种操作方法,将上述另一种未饱和的溶液变为饱和,下列说法正确的是CD(填字母序号,可多选).
A.溶液中溶质的质量一定增加 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可降低温度或增加溶质.
19.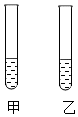 某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
 某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )| A. | 甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液 | |
| B. | 乙试管底部有固体,说明乙试管中的溶液为浓溶液 | |
| C. | 此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和 | |
| D. | 该实验现象说明该温度下蔗糖的溶解度比熟石灰大 |


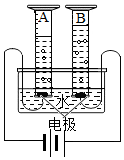 如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气.
如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气.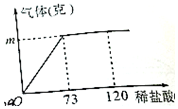 10克碳酸钙与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示
10克碳酸钙与稀盐酸反应,加入稀盐酸的质量与生成气体的质量关系如图所示