题目内容
7.如表所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的有关数据如下:| 气体发生装置内物质的总质量(g) | |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
(2)反应生成氧气的质量为0.8g(结果精确到0.1g,下同)
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程.
分析 (1)根据用过氧化氢溶液和二氧化锰制取氧气中二氧化锰起催化作用进行解答;
(2)根据质量守恒定律可以知道反应前后减少的质量即为生成氧气的质量,可以据此解答;
(3)根据生成氧气的质量结合过氧化氢分解的化学方程式可以求算出过氧化氢的质量进行解答.
解答 解:(1)用过氧化氢溶液和二氧化锰制取氧气中二氧化锰起催化作用;故填:催化作用;
(2)根据质量守恒定律可以知道反应前后减少的质量即为生成氧气的质量,即为:35.6g-34.8g=0.8g;故填:0.8;
(3)设参加反应的过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}=\frac{32}{0.8g}$
解得:x=1.7g
答:参加反应的过氧化氢的质量为1.7g.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.元素周期律和元素周期表是研究化学的重要工具.下表是元素周期表的部分信息.
请认真分析表中信息,回答下列问题.
(1)地壳中含量最多的金属元素的原子序数是13;
(2) 表示的是S2- (写粒子符号);
表示的是S2- (写粒子符号);
(3)原子序数为9和20的两种元素组成的化合物是CaF2(写化学式);
(4)从原子结构角度看,同一周期元素的原子具有相同的电子层数.
(5)图 是氯元素的原子结构示意图,图上表中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似.由此推测,氟原子在化学反应中易得(填“得”或“失”)个电子.“②”处元素在化合物中显+2 价.
是氯元素的原子结构示意图,图上表中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似.由此推测,氟原子在化学反应中易得(填“得”或“失”)个电子.“②”处元素在化合物中显+2 价.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第二 周期 | 3 Li 锂 7 | 4 Be 铍 9 | 5 B 硼 11 | ① | 7 N 氮 14 | 8 O 氧 16 | 9 F 氟 19 | 10 Ne 氖 20 |
| 第三 周期 | 11 Na 钠 23 | ② | 13 Al 铝 27 | 14 Si 硅 28 | ③ | 16 S 硫 32 | 17 Cl 氯 35.5 | 18 Ar 氩 40 |
(1)地壳中含量最多的金属元素的原子序数是13;
(2)
 表示的是S2- (写粒子符号);
表示的是S2- (写粒子符号);(3)原子序数为9和20的两种元素组成的化合物是CaF2(写化学式);
(4)从原子结构角度看,同一周期元素的原子具有相同的电子层数.
(5)图
 是氯元素的原子结构示意图,图上表中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似.由此推测,氟原子在化学反应中易得(填“得”或“失”)个电子.“②”处元素在化合物中显+2 价.
是氯元素的原子结构示意图,图上表中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似.由此推测,氟原子在化学反应中易得(填“得”或“失”)个电子.“②”处元素在化合物中显+2 价.
18.将Fe粉置于Ag(NO3)2和Zn(NO3)2的混合溶液中,待反应完毕后,所得金属中一定含有的是( )
| A. | Fe | B. | Fe,Ag | C. | Fe,Ag,Zn | D. | Ag |
15.下列物质,不能由金属单质和盐酸直接反应生成的是( )
| A. | ZnCl2 | B. | AlCl3 | C. | MgCl2 | D. | FeCl3 |
2.下列有关物质构成的说法不正确的是( )
| A. | 物质可由分子、原子或离子构成 | |
| B. | 水加热变成水蒸气,说明分子能分成原子 | |
| C. | 液氧和氧气都能助燃--同种分子化学性质相同 | |
| D. | 某元素的原子,其原子核内含有21个质子,31个中子,则其原子的核外电子数为21 |
12.绿色植物进行光合作用吸收的是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
16.根据如图所示的实验A、B、C,回答下题
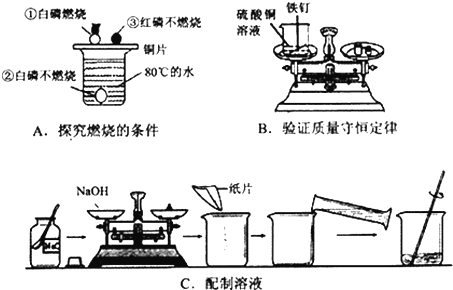
(1)实验A中,铜片上的红磷没有燃烧,说明燃烧需要达到着火点
(2)实验B中,能充分证明质量守恒定律的现象是天平仍保持平衡
(3)实验C中的一处明显错误是氢氧化钠放在纸片上称量如果量取水时,仰视读数,配得的氢氧化钠溶液中溶质的质量分数将偏小(填“偏大”、“偏小”或“不变”),配置好的氢氧化钠溶液必须密封保存,原因是氢氧化钠会和空气中的CO2反应而变质.写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O
(4)某兴趣小组同学为了验证实验室中久置的氢氧化钠是否变质,进行了如下表的实验.请你与他们一起完成以下验证实验:

(1)实验A中,铜片上的红磷没有燃烧,说明燃烧需要达到着火点
(2)实验B中,能充分证明质量守恒定律的现象是天平仍保持平衡
(3)实验C中的一处明显错误是氢氧化钠放在纸片上称量如果量取水时,仰视读数,配得的氢氧化钠溶液中溶质的质量分数将偏小(填“偏大”、“偏小”或“不变”),配置好的氢氧化钠溶液必须密封保存,原因是氢氧化钠会和空气中的CO2反应而变质.写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O
(4)某兴趣小组同学为了验证实验室中久置的氢氧化钠是否变质,进行了如下表的实验.请你与他们一起完成以下验证实验:
| 设计实验 | 实验现象 | 结论 |
| 为检验是否变质,取少量固体加水溶解后,滴入足量稀盐酸; | 产生大量的气泡 | 已变质 |
| 为进一步探究是否全部变质,另取少量固体加水溶解后,加入过量 的 CaCl2溶液,完全反应后过滤,往滤液中滴加酚酞. | 酚酞溶液变红色 | 部分变质 |
17.如图所示各项实验中,所用试剂及实验操作均正确的是( )
| A. | 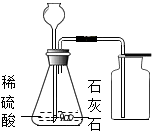 制取CO2 | B. |  加热固体 | ||
| C. |  制取氧气 | D. |  除去O2中的水蒸气 |
 水是最普通、最常见的物质之一.
水是最普通、最常见的物质之一.