题目内容
3.类比法是学习化学的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,而且仅生成氧化物.某校研究性学习小组对此展开探究:(1)小明首先根据草酸中含氢、氧元素,推测生成物中含有水.
(2)小明又对草酸分解生成的气体成分进行如下探究:
【提出假设】假设1:该气体只含有二氧化碳 假设2:该气体只含有一氧化碳
假设3:该气体是二氧化碳和一氧化碳的混合物
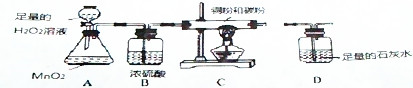
(3)【设计实验方案】取少量氧化铁红色粉末放入硬质玻璃管中,设法排出装置中原有空气后,再将该气体依次通过装置A、B、C、D.对C加热(装置如下图).请你完成下表:

(4)【进行实验】通过实验及现象分析,确认假设3成立.
(5)【反思与评价】
①实验过程中,A试管中发生反应的方程式是CO2+Ca(OH)2═CaCO3↓+H2O;硬质玻璃管内发生反应的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,现象为红色粉末变黑.
②B装置利用浓硫酸的吸水性干燥气体;A与D装置所盛物质相同,下列说法正确的是Ⅰ.
Ⅰ.由于A、D所处位置不同,其作用也就不同
Ⅱ.虽然A、D所处位置不同,但作用完全相同
Ⅲ.设置D装置的主要目的是检测草酸分解产物中是否含有二氧化碳.
分析 根据质量守恒定律,反应前后元素的种类不变,判断元素和物质的组成;二氧化碳用澄清的石灰水检验;C装置中红棕色固体粉末是氧化铁,一氧化碳还原氧化铁,得到单质铁和而二氧化碳.一氧化碳有毒,因此用一氧化碳做还原剂时,要有尾气处理装置.由实验探究可知:草酸在加热的条件下,生成水、二氧化碳和一氧化碳.
解答 解:(1)由草酸分解能生成水,再根据质量守恒定律,可推出草酸中一定含有氢元素和氧元素;故填:氢、氧;
(5)①二氧化碳一般用澄清的石灰水来检验,实验现象是澄清的石灰水变浑浊,故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
C装置中红棕色固体粉末是氧化铁,一氧化碳还原氧化铁,得到单质铁和而二氧化碳,配平即可.
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;红色粉末变黑;
②浓硫酸具有吸水性,可用来干燥气体;AD位置不同,作用也不相同,A检验草酸分解产物中含有二氧化碳,D是用来检验草酸分解产物中是否含一氧化碳(因为一氧化碳在加热的条件下与氧化铁反应生成二氧化碳).故填:吸水;Ⅰ.
点评 本考点属于实验探究题,探究草酸的性质和变化规律,还有气体的检验和化学方程式的书写,综合性比较强.本题根据题目提供的信息,结合实验探究的一般步骤和酸的性质等知识来解决,还要注意化学方程式的书写和配平.本考点主要出现在实验题中.

练习册系列答案
相关题目
13.某同学的实验报告中,有以下实验数据,其中不合理的是( )
| A. | 用pH试纸测得溶液的pH值为3.5 | B. | 用体温计测得体温为37.5℃ | ||
| C. | 用10ml量筒量取5.6ml稀盐酸 | D. | 用托盘天平称得12.8g食盐 |
18.一壶水烧开后,壶盖被顶开,这是因为( )
| A. | 水由液态变成气态,分子间隔变大 | B. | 水分解成氢气和氧气 | ||
| C. | 水分子变大了 | D. | 水分子数目增多 |