题目内容
3.为研究酸的性质,某研究小组进行了如下探究.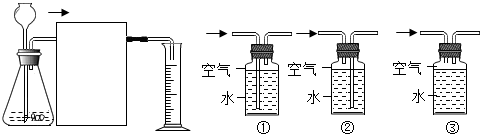
(1)小刚将颗粒大小相同的纯锌粒和粗锌分别加入相同浓度的稀硫酸中,写出锌与硫酸反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)小刚仔细观察后发现纯锌粒和硫酸的反应明显比粗锌粒慢,通过查阅资料小刚得知粗锌中含有一些不活泼金属,她猜想可能是粗锌中不活泼金属促进了锌和硫酸的反应.为了验证小刚的猜想,你认为应该在盛有纯锌粒和稀硫酸的试管中,加入少量的下列哪种物质?B.
A.HCl B.CuCl2 C.NaCl D.CaCl2
(3)实验中小刚发现加入上述所选物质,纯锌和稀硫酸的反应都有不同程度的加快,请你分析可能的原因是什么?四种溶液中的Cl-对溶液起了促进作用.
(4)小刚想通过用一定质量粗锌和足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度设计了如图所示的实验装置.在虚线框中应接入图中的②,广口瓶上方残留的空气不会(填“会”或“不会”)对氢气体积的测量造成影响.
分析 (1)根据锌与硫酸反应生成硫酸锌和氢气,写出反应的化学方程式解答;
(2)根据金属活动性顺序解答;
(3)根据题中信息分析解答;
(4)根据氢气的密度比水的小解答.
解答 解:(1)锌粒与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(2)由金属活动性顺序可知:钠、钙都比锌活泼,铜不如锌活泼,为了验证小刚的猜想,应该在盛有纯锌粒和稀硫酸的试管中,加入少量的CuCl2;
(3)实验中小刚发现加入上述所选物质,纯锌和稀硫酸的反应都有不同程度的加快,可能的原因是四种溶液中的Cl-对溶液起了促进作用;
(4)氢气的密度比水的小,收集氢气时应短进,故用一定质量粗锌和足量的硫酸反应,测量生成氢气的体积来计算粗锌的纯度设计了如图所示的实验装置.在虚线框中应接入图中的②,因为通过排出的水来测量氢气的体积,广口瓶上方残留的空气不会对氢气体积的测量造成影响.
答案:
(1)Zn+H2SO4═ZnSO4+H2↑.
(2)B;
(3)四种溶液中的Cl-对溶液起了促进作用;
(4)②;不会.
点评 本题主要考查化学实验的方案设计与评价,在解此类题时,首先分析题中考查的问题,然后结合所给的知识和学过的知识进行分析解答.

练习册系列答案
相关题目
18.海洋中蕴藏着丰富的化学资源,如NaCl、MgCl2、CaCl2等物质.从海水中提取金属镁的主要流程如土1: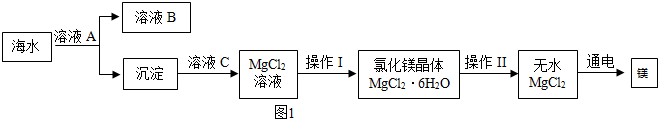
(1)电解熔融的无水MgCl2可以得到金属镁.该反应属于基本反应类型中的分解反应.
(2)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来.结合表中数据分析,为了使氯化镁转化为沉淀,应加入的溶液A可能是Ca(OH)2溶液(或NaOH溶液).
室温下几种物质的溶解度
(3)结合MgCl2的溶解度曲线如图2分析,操作I:蒸发浓缩、降温结晶、过滤.
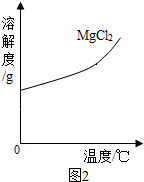

(1)电解熔融的无水MgCl2可以得到金属镁.该反应属于基本反应类型中的分解反应.
(2)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来.结合表中数据分析,为了使氯化镁转化为沉淀,应加入的溶液A可能是Ca(OH)2溶液(或NaOH溶液).
室温下几种物质的溶解度
| 物质 | MgCO3 | CaCO3 | Mg(OH)2 | Ca(OH)2 |
| 溶解度/g | 0.01 | 0.0013 | 0.0029 | 0.16 |

9.“达菲”是治疗甲型H1N1流感的有效药物,其生产原料是香料八角中所含有的一种重要成分-莽草酸,莽草酸的化学式为C7H10O5,下列有关莽草酸的说法正确的是( )
| A. | 莽草酸的相对分子质量为174克 | |
| B. | 莽草酸中含有7个碳元素、10个氢元素、5个氧元素 | |
| C. | 1个莽草酸分子中含有22个原子 | |
| D. | 莽草酸中碳、氢、氧三种元素的质量比是:7:10:5 |
 如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题:
如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题: 如图所示的是检验氢气纯度的操作.
如图所示的是检验氢气纯度的操作. 菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图(1)所示,已知菱铁矿中杂质不参加反应,且难溶于水.请计算:
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图(1)所示,已知菱铁矿中杂质不参加反应,且难溶于水.请计算: