题目内容
18.海洋中蕴藏着丰富的化学资源,如NaCl、MgCl2、CaCl2等物质.从海水中提取金属镁的主要流程如土1: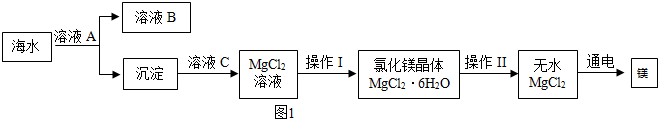
(1)电解熔融的无水MgCl2可以得到金属镁.该反应属于基本反应类型中的分解反应.
(2)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来.结合表中数据分析,为了使氯化镁转化为沉淀,应加入的溶液A可能是Ca(OH)2溶液(或NaOH溶液).
室温下几种物质的溶解度
| 物质 | MgCO3 | CaCO3 | Mg(OH)2 | Ca(OH)2 |
| 溶解度/g | 0.01 | 0.0013 | 0.0029 | 0.16 |
分析 (1)据反应类型的判定即化合反应、分解反应、置换反应和复分解反应的判定解答;
(2)氯化镁转化为氢氧化镁需要加入碱液,验证MgCl2已完全转化为Mg(OH)2的方法是取滤液滴入Ca(OH)2溶液(或NaOH溶液)是否有沉淀生成;
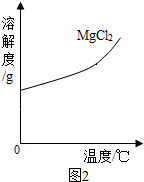
(3)根据氯化镁的溶解度随温度的变化情况分析结晶的方法.
解答 解:(1)据反应反应的概念,电解熔融的无水MgCl2可以得到金属镁和氯气,反应属于一变多,故此反应属于基本反应类型中的分解反应;
(2)氯化镁转化为氢氧化镁需要加入碱液以提供氢氧根,此处选择过量的Ca(OH)2溶液(或NaOH溶液)进行反应,目的是让所取海水中的氯化镁全部转化为氢氧化镁沉淀;
(3)由于氯化镁的溶解度随温度的升高而增大,所以,从氯化镁溶液中取得氯化镁晶体,应选择降低温度结晶的方法.
故答案为:(1)分解; (2)Ca(OH)2溶液(或NaOH溶液);(3)降温结晶.
点评 本题难度不大,明确工业上制取金属镁的反应流程、碱的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列对有关实验现象的描述正确的是( )
| A. | 铁丝在空气中燃烧时,火星四射,有黑色物质生成 | |
| B. | 硫在氧气中燃烧时,产生蓝紫色火焰 | |
| C. | 甲烷在氧气中燃烧时,有水和二氧化碳生成 | |
| D. | 铝丝浸入硫酸铜溶液表面有红色的铜生成 |
 在自来水消毒过程中,通常要发生化学反应,其反应的微观过程可用如图表示:(图注:●表示氯原子○表示氧原子●表示氢原子)
在自来水消毒过程中,通常要发生化学反应,其反应的微观过程可用如图表示:(图注:●表示氯原子○表示氧原子●表示氢原子)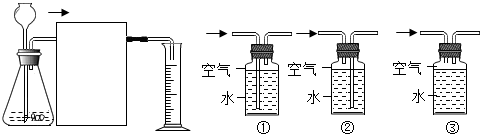
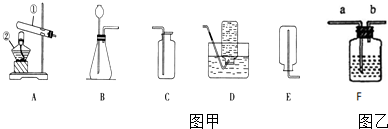
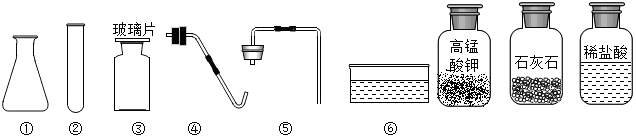
 实验仪器的安全使用非常重要.
实验仪器的安全使用非常重要.