题目内容
10.小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20g此氢氧化钠溶液于烧杯中,向其中滴加溶质质量分数为7.3%的稀盐酸,并随时用pH计(一种测定溶液pH的仪器)测定反应后溶液的pH.记录的数据如下表:| 加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 反应后溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(2)请计算所测氢氧化钠溶液中溶质的质量分数.
分析 (1)根据pH值来决定酸碱的反应情况从而决定溶液中的溶质成分;
(2)根据恰好反应时消耗的盐酸质量来计算氢氧化钠的质量即可解答.
解答 解:
(1)当滴加稀盐酸的质量为9.8g时,PH=12.1,说明溶液显碱性,即氢氧化钠有剩余,故溶液中的溶质是生成的氯化钠和剩余的氢氧化钠;
(2)10g溶质质量分数为7.3%的稀盐酸中溶质质量=10g×7.3%=0.73g
设20.0g氢氧化钠溶液中溶质的质量为x,
HCl+NaOH=NaCl+H2O
36.5 40
0.73g x
$\frac{36.5}{0.73g}=\frac{40}{x}$
x=0.8g
所测氢氧化钠溶液中溶质的质量分数=$\frac{0.8g}{20g}×$100%=4%
答案:
(1)碱 NaOH、NaCl
(2)所测氢氧化钠溶液中溶质的质量分数为4%
点评 本题主要考查了学生根据化学方程式进行简单计算的能力,涉及的为题较多,但难度不大,关键是解题步骤要规范.

练习册系列答案
相关题目
20.空气中能供给动植物呼吸的是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 水蒸气 |
1.“玻璃钢”现在已经成为世界上产量最大、用途最广的一种材料.请问:“玻璃钢”属于哪种材料( )
| A. | .金属材料 | B. | 无机非金属材料 | C. | 合成材料 | D. | 复合材料 |
5.在实验室里用括号中的试剂或方法鉴别下列各组物质,正确的是( )
| A. | 硬水和软水(品尝) | B. | NaOH固体和NaCl固体(水) | ||
| C. | N2和CO2(燃着的木条) | D. | 羊毛纤维与合成纤维(看颜色) |
15.某同学设计了探究Fe、Cu、Ag三种金属活动性顺序的实验方案,仅用组内试剂,无法完成的是( )
| A. | Fe、Cu、Ag、稀硫酸 | B. | Cu、FeSO4溶液、AgNO3溶液 | ||
| C. | Fe、Ag、CuSO4溶液 | D. | Fe、Cu、稀硫酸、AgNO3溶液 |
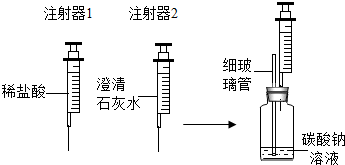 碳酸钠与盐酸的反应是分两步进行的,第一步反应的化学方程式为:Na2CO3+HCl═NaCl+NaHCO3.为验证该反应分两步进行.如图所示进行实验(装置气密性良好).
碳酸钠与盐酸的反应是分两步进行的,第一步反应的化学方程式为:Na2CO3+HCl═NaCl+NaHCO3.为验证该反应分两步进行.如图所示进行实验(装置气密性良好).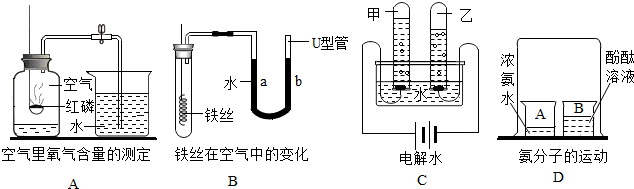
 点燃一根蜡烛,并进行下列有关实验.回答:
点燃一根蜡烛,并进行下列有关实验.回答: