题目内容
19.为了除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,将粗盐溶于水,然后进行下列五步操作:①过滤;②加过量的氢氧化钠溶液;③加适量盐酸;④加过量的碳酸钠溶液;⑤加过量的氯化钡溶液;正确的操作顺序是②⑤④①③或⑤②④①③.分析 根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答.
解答 解:镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,再进行过滤,最后再加入适量盐酸除去反应剩余的氢氧根离子和碳酸根离子,故正确的顺序为:②⑤④①③或⑤②④①③.
故答案为:②⑤④①③或⑤②④①③.
点评 本题难度较大,考查了粗盐提纯中离子的除杂,除去多种杂质离子时,要考除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
9.氢溴酸(HBr)的化学性质与盐酸非常相似,下列物质中不可与氢溴酸发生反应的是( )
| A. | Fe | B. | Ag | C. | Fe2O3 | D. | NaHCO3 |
10.小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20g此氢氧化钠溶液于烧杯中,向其中滴加溶质质量分数为7.3%的稀盐酸,并随时用pH计(一种测定溶液pH的仪器)测定反应后溶液的pH.记录的数据如下表:
(1)当加入稀盐酸的质量为9.8g时,反应后的溶液呈碱性(填“酸”、“碱”或“中”),该溶液中的溶质是NaOH、NaCl;
(2)请计算所测氢氧化钠溶液中溶质的质量分数.
| 加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 反应后溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(2)请计算所测氢氧化钠溶液中溶质的质量分数.
7.下列关于化学反应的实验现象描述不正确的是( )
| A. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成黑色固体 | |
| B. | 木炭在氧气中燃烧发出白光,生成黑色固体 | |
| C. | 点燃羊毛纤维时会闻到烧焦羽毛气味 | |
| D. | 将二氧化碳气体通入澄清石灰水中,澄清石灰水变浑浊 |
4.某无色气体可能含有CH4、CO、H2中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全)①无色气体在足量氧气中燃烧;②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6g;③再将剩余气体通过盛有NaOH溶液的洗气瓶,装置增重4.4g;下列推断正确的是( )
| A. | 该气体可能只含有CO、H2 | B. | 该气体可能只含有CH4、CO | ||
| C. | 该气体一定只含有CH4 | D. | 该气体一定只含有CH4、H2 |
11.化学实验是科学探究的重要学习方式.下列实验操作正确的是( )
| A. | 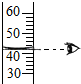 量取液体体积 | B. |  给试管内液体加热 | ||
| C. |  铁丝在氧气中燃烧 | D. | 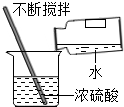 稀释浓硫酸 |
