题目内容
19.将20g质量为20%的氢氧化钠溶液与80g某硫酸溶液混合,充分反应后溶液呈中性.求所得溶液中溶质的质量分数.分析 反应后溶液呈中性,说明氢氧化钠溶液和硫酸恰好完全反应,根据参加反应的氢氧化钠溶液的质量及其溶质的质量分数,由反应的化学方程式计算出所得溶液中溶质的质量,进而由溶质的质量分数计算公式计算出反应后所得溶液中溶质的质量分数.
解答 解:20g质量为20%的氢氧化钠溶液中氢氧化钠的质量为:20g×20%=4g
设反应后所得溶液中溶质的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O
80 142
4g x
$\frac{80}{4g}$=$\frac{142}{x}$
解得:x=7.1g
所得溶液中溶质的质量分数为:$\frac{7.1g}{20g+80g}$×100%=7.1%.
答:所得溶液中溶质的质量分数为7.1%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题.

练习册系列答案
相关题目
7.某条件下,6.6gC3H8与22.4gO2恰好完全反应,生成10.8gH2O、15.4gCO2和物质X,则该反应的化学方程式中O2与X的化学计量数之比为( )
| A. | 2:1 | B. | 7:1 | C. | 4:7 | D. | 16:7 |
11.下列描述错误的是( )
| A. | 化学变化中原子是最小的粒子 | |
| B. | 化学反应的本质是分子的破裂,原子的重新组合 | |
| C. | 分子是由原子构成的 | |
| D. | 分子可以再分,而原子不可再分 |
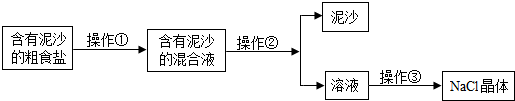
9.用括号内的物质或方法除去下列各组中的杂质,其中错误的是( )
| A. | 氢氧化钠溶液中混有少量的碳酸钠(适量的氢氧化钙溶液) | |
| B. | 铜粉中混有铁粉(用磁铁吸引) | |
| C. | 氧化钙中混有少量的碳酸钙(适量盐酸) | |
| D. | 二氧化碳混有少量的一氧化碳(灼热的氧化铜) |
 在一烧杯中盛有22.3g Na2CO3和NaCl组成的固体混合物,加43.1g水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题:(H-1;Cl-35.5;Na-23;C-12;O-16)
在一烧杯中盛有22.3g Na2CO3和NaCl组成的固体混合物,加43.1g水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题:(H-1;Cl-35.5;Na-23;C-12;O-16)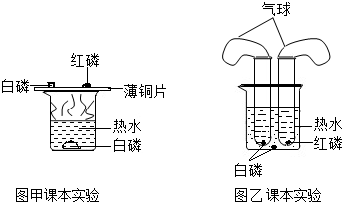 小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中
小明与同学一起对教材中“燃烧的条件”这个实验(图甲)进行了如下改进(图乙):去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个气球,用线固定,然后将两支大使馆同时浸在盛有热水的烧杯中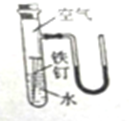 如图是某研究的实验装置,几天以后:
如图是某研究的实验装置,几天以后: