题目内容
13.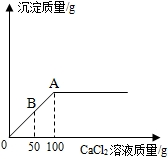 (1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示:
(1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示:(1)B点处所得溶液中溶质有氢氧化钠、氯化钠、碳酸钠.(填物质名称)
(2)求待测溶液中Na2CO3的质量分数.
分析 (1)碳酸钠与氯化钙可以生成碳酸钙沉淀和氯化钠,而关系图中B点处于反应的中间状态,因此,此时待测溶液中的碳酸钠未完全反应.据此推断B点所表示的溶液中溶质;
(2)待测溶液中Na2CO3的质量分数=$\frac{20g待测溶液中碳酸钠质量}{待测溶液质量20g}$×100%,所以需要根据碳酸钠完全反应时所消耗氯化钙质量计算碳酸钠的质量.椐关系图可知:A点时滴加100g氯化钙溶液恰好与碳酸钠完全反应.
解答 解:(1)由关系图可知:B点时碳酸钠未完全反应,因此所得溶液中含有未完全反应的碳酸钠和反应生成的氯化钠及不参与反应的氢氧化钠;
故答案为:氢氧化钠、氯化钠、碳酸钠;
(2)设待测溶液中Na2CO3的质量分数为x,则:
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
20g×x 100g×1.11%
$\frac{106}{20g×x}=\frac{111}{100g×1.11%}$
x=5.3%
答:待测溶液中Na2CO3的质量分数为5.3%
点评 反应与图形相结合类问题,根据图形分析反应的进程是进行答题的基础,图形中的拐点往往是恰好完全反应点.

练习册系列答案
相关题目
3.除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )
| A. | CaCO3固体(CaO固体)--高温煅烧 | |
| B. | CO2(CO)--通过灼热的氧化铜 | |
| C. | CO(CO2)--通过灼热的炭层 | |
| D. | KCl溶液(CaCl2溶液)--滴加碳酸钠溶液至恰好完全反应,过滤 |
4.下列关于浓硫酸的描述错误的是( )
| A. | 溶于水时放出大量的热 | B. | 有强烈的腐蚀性 | ||
| C. | 浓硫酸必须密封保存 | D. | 可在量筒中用浓硫酸配制稀硫酸 |
2.化学与健康--从化学的视角看食品添加剂.
请用化学符号或化学式填空:
①写出碳酸氢钠的化学式NaHCO3;它与盐酸反应生成的气体化学式是CO2;
②写出铁与盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑;
③写出食盐与硝酸银溶液反应的化学方程式NaCl+AgNO3═NaNO3+AgCl↓;
④亚硝酸钠(NaNO2) 中的氮元素化合价是+3;它与硝酸银发生复分解反应,则反应生成的浅黄色沉淀化学式是AgNO2.
| 添加剂名称 | 主要化学性质及在体内变化 |
| 碳酸氢钠 | 无毒、弱碱性,易与胃酸反应,加热分解成碳酸钠、水和二氧化碳 |
| 铁 (还原性铁粉) | 比较活泼的金属,能与胃酸反应 |
| 食盐 | 易溶、中性,与硝酸银溶液反应生成白色沉淀 |
| 亚硝酸钠 | 易溶、水溶液显碱性,跟硝酸银反应生成浅黄色沉淀 |
①写出碳酸氢钠的化学式NaHCO3;它与盐酸反应生成的气体化学式是CO2;
②写出铁与盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑;
③写出食盐与硝酸银溶液反应的化学方程式NaCl+AgNO3═NaNO3+AgCl↓;
④亚硝酸钠(NaNO2) 中的氮元素化合价是+3;它与硝酸银发生复分解反应,则反应生成的浅黄色沉淀化学式是AgNO2.
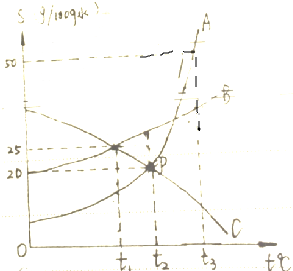 .
. 普通黄铜仅由铜和锌组成,现有一块黄铜样品的质量为50.00g,某学习小组利用一种未知浓度的稀盐酸来测定锌铜合金中铜的质量分数.实验中样品与酸充分反应,样品的质量变化情况如图所示.
普通黄铜仅由铜和锌组成,现有一块黄铜样品的质量为50.00g,某学习小组利用一种未知浓度的稀盐酸来测定锌铜合金中铜的质量分数.实验中样品与酸充分反应,样品的质量变化情况如图所示. 实验室常用盐酸和石灰石反应制取二氧化碳.
实验室常用盐酸和石灰石反应制取二氧化碳.