题目内容
5. 实验室常用盐酸和石灰石反应制取二氧化碳.
实验室常用盐酸和石灰石反应制取二氧化碳.(1)该反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.将反应后的气体通入石灰水中,有时会有在开始一段时间内未发现石灰水变浑浊的现象,其原因可能是盐酸中挥发出的氯化氢气体进入澄清石灰水中.
(2)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某小组经研究,用如图所示方法成功制得了大量CO2(反应物为稀硫酸和石灰石).
①当稀硫酸和石灰石反应,在硫酸溶液中加入的氯化铵和对溶液加热,其目的都是增大硫酸钙在溶液中的溶解度.
②改进实验是为了收到更好的实验效果,按上图的方法,你认为相比用盐酸和石灰石反应,其改进的出发点是证明利用稀硫酸和石灰石也可以制取二氧化碳.
分析 (1)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
盐酸易挥发,生成的二氧化碳中常常混有少量的氯化氢气体;
(2)温度升高时,磷酸钙的溶解度会增大;
实验装置不同,制取气体的反应物可以不同.
解答 解:(1)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
在开始一段时间内未发现石灰水变浑浊,其原因可能是盐酸中挥发出的氯化氢气体进入澄清石灰水中,形成的稀盐酸先和氢氧化钙反应生成氯化钙和水.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;盐酸中挥发出的氯化氢气体进入澄清石灰水中.
(2)①当稀硫酸和石灰石反应,在硫酸溶液中加入的氯化铵和对溶液加热,其目的都是增大硫酸钙在溶液中的溶解度.
故填:增大硫酸钙在溶液中的溶解度.
②相比用盐酸和石灰石反应,其改进的出发点是证明在一定条件下,利用稀硫酸和石灰石也可以制取二氧化碳.
故填:证明利用稀硫酸和石灰石也可以制取二氧化碳.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.除去下列物质中的杂质,所用的试剂和方法不正确的是( )
| 题号 | 物质(杂质) | 所用试剂和方法 |
| A | 碳酸钙(熟石灰) | 加入过量稀盐酸、过滤 |
| B | 一氧化碳(二氧化碳) | 将气体通过氢氧化钠溶液、干燥 |
| C | 铜粉(铁粉) | 加入过量的稀盐酸、过滤、洗涤、烘干 |
| D | 二氧化锰(氯化钾) | 溶解、过滤、洗涤、烘干 |
20.类推是学习知识的一种重要方法,以下类推正确的是( )
| A. | H2、CO与氧气混合点燃会发生爆炸,所以点燃可燃性气体前一定要检验其纯度 | |
| B. | CO2、SO2都能与碱溶液反应,由此可知碱能与所有非金属氧化物反应 | |
| C. | 置换反应都是氧化还原反应,所以氧化还原反应都是置换反应 | |
| D. | 有机物都含碳元素,所以含碳元素的化合物都是有机物 |
10.食品安全备受人们关注,下列做法危及人的生命的是( )
| A. | 长期饮用白开水 | B. | 用甲醛溶液浸泡海鲜 | ||
| C. | 食品袋里充入氮气延长食品保质期 | D. | 食用蔬菜以补充维生素 |
14.酸与碱作用生成盐和水的反应,叫做中和反应.下列应用与中和反应原理无关的是( )
| A. | 用熟石灰和硫酸铜配制波尔多液 | |
| B. | 服用含Mg(OH)2的药物治疗胃酸过多 | |
| C. | 施用熟石灰改良酸性土壤 | |
| D. | 用氨水与工厂排放的含硫酸的废水反应制氮肥 |
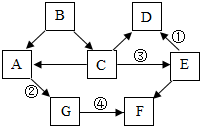 A-G表示初中化学的常规物质,它们之间的转化如图所示(部分反应物、生成物和反应条件已罗去).已知:A、B、C、F均为气体,且C、F可做燃料,D和E为常见金属,且E是世界年产量最高的金属,常温下,G为无色无味液体,请回答下列问题
A-G表示初中化学的常规物质,它们之间的转化如图所示(部分反应物、生成物和反应条件已罗去).已知:A、B、C、F均为气体,且C、F可做燃料,D和E为常见金属,且E是世界年产量最高的金属,常温下,G为无色无味液体,请回答下列问题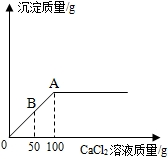 (1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示:
(1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示: 陈程同学经常采用构建知识网络的方法学习化学.如他将某些物质相互关系构建为如图所示的知识网络图(“→”表示这种物质转化为另一种物质).回答下列问题:
陈程同学经常采用构建知识网络的方法学习化学.如他将某些物质相互关系构建为如图所示的知识网络图(“→”表示这种物质转化为另一种物质).回答下列问题: 如图是某品牌化肥中的部分说明.根据相关部门规定,若物质的主要成分纯度达到96%,就达到一级品的要求,根据计算说明,该品牌化肥的说明是否属实?
如图是某品牌化肥中的部分说明.根据相关部门规定,若物质的主要成分纯度达到96%,就达到一级品的要求,根据计算说明,该品牌化肥的说明是否属实?