题目内容
13.某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置,其中过氧化钠可作供氧剂”感到非常好奇,设计实验进行探究.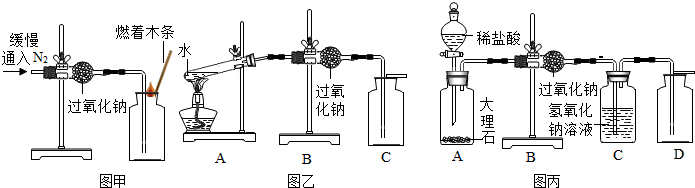
【提出问题】过氧化钠能与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH=Na2CO3+H2O.用氢氧化钠溶液吸收二氧化碳效果较好.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气.
(1)实验操作如图甲所示.
(2)实验现象及结论:观察到燃着木条熄灭现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.
(1)同学们在老师的指导下设计了如图乙所示装置进行实验,并用带火星的木条检验.其中A装置的作用是提供水蒸气.
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气的支持燃烧的性质.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
(1)同学们在老师的指导下设计了如图丙所示装置.
(2)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | \ | 装置的气密性良好. |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | A装置中观察到的现象有有气泡冒出,固体逐渐减少. | A装置中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.
分析 【进行实验】实验Ⅰ:(2)如果过氧化钠与氮气发生反应生成氧气,则燃着的木头燃烧更旺;
实验Ⅱ:(1)根据题意判断;根据是否有无新物质生成判断物质的变化;
实验Ⅲ:(2)②大理石和稀盐酸反应生成二氧化碳气体判断反应现象;
【实验反思】根据生成的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气进行解答;
解答 解:【进行实验】实验Ⅰ:(2)如果过氧化钠与氮气发生反应生成氧气,则燃着的木头燃烧更旺,如没反应,则燃着的木条熄灭,故填:燃着木条熄灭
实验Ⅱ:(1)由题意知,A装置是把水加热至沸腾产生水蒸气,所以A装置的作用是提供水蒸气,故填:提供水蒸气;
(2)过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气支持燃烧的性质;
实验Ⅲ:(2)②大理石和稀盐酸反应生成氯化钙、水和二氧化碳,所以反应现象是有气泡产生,同时大理石逐渐减小;C装置作用是除去没反应掉的二氧化碳,能收集到较纯的氧气.故填:有气泡冒出,固体逐渐减少;CaCO3+2HCl=CaCl2+H2O+CO2↑;除去二氧化碳
【实验反思】因为生成的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气,故应先干燥二氧化碳,在和过氧化钠反应,故填:二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.
故本题答案为:
【进行实验】实验Ⅰ:(2)燃着木条熄灭;
实验Ⅱ:(1)提供水蒸气;(2)支持燃烧的;
实验Ⅲ:(2)
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | \ | 装置的气密性良好. |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | A装置中观察到的现象有 有气泡冒出,固体逐渐减少. | A装置中发生反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
点评 本题考查了过氧化钠与二氧化碳的反应及其反应产物氧气和碳酸钠的检验,完成此题,可以依据题干提供的信息以及已有的知识进行.

练习册系列答案
相关题目
15.规范的操作是化学实验成功的保障.下列实验操作中正确的是( )
| A. | 测定溶液的PH时,将试纸直接放入待测液中 | |
| B. | 将固体药品直接放在天平的托盘上称量 | |
| C. | 不慎将浓碱溶液沾到皮肤上,立即用大量水冲洗,再涂上硫酸 | |
| D. | 实验室用CO还原氧化铁时,先通CO,再点燃加热氧化铁的酒精喷灯 |
1.某同学在研究“铜绿”性质的实验时,实验操作示意图如图,其中有错误的是( )
| A. |  加入“铜绿” | B. |  倾倒稀盐酸 | C. |  加热“铜绿” | D. |  洗涤试管 |
2.生活中的下列现象,能说明气体的溶解度随压强变化而变化的是( )
| A. | 夏天,鱼塘中的鱼常常会浮在水面呼吸 | |
| B. | 烧开水时,沸腾前水中有气泡产生 | |
| C. | 打开“七喜”饮料瓶盖会有大量气泡冒出 | |
| D. | 喝了汽水以后,常常会打嗝 |