题目内容
14.海洋是个巨大的资源宝库,充分利用海洋资源体现了人类改造物质的智慧,如海水晒盐、海水制碱、海水淡化、海水制镁等.(1)从海水中提取食盐的方法主要为盐田法,这是一种古老而至今仍广泛沿用的方法.海水晒盐的流程如图1:
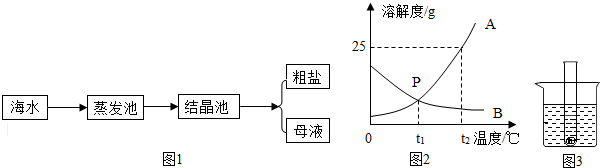
海水晒盐后得到的母液是当时温度下氯化钠的饱和溶液(填“饱和”或“不饱和”).
(2)图2是A、B物质的溶解度曲线,回答下列问题:
①写出P点的意义在t1℃时AB的溶解度相等(t1℃时AB两饱和溶液的溶质质量分数相等)(只写一条即可).
②t2℃时,A 的饱和溶液中溶质的质量分数为20%.
③将t1℃时A的饱和溶液升高温度,溶液中溶质的质量分数不变( 填“变大”、“变小”或“不变”).
(3)t2℃时,一小试管内盛有B的饱和溶液,试管底部还存有少许B固体,将小试管放入盛有水的烧杯中(如图3所示),向烧杯中的水中加入一种固体物质X,发现小试管内的固体物质逐渐溶解,根据所学知识推断所加物质X可能是NH4NO3(填化学式).
分析 根据已有的饱和溶液的形成、溶解度曲线的意义进行分析解答即可.
解答 解:(1)海水晒盐后得到的母液是当时温度下氯化钠的饱和溶液,故填:饱和;
(2)①P点表示在t1℃时AB的溶解度相等(t1℃时AB两饱和溶液的溶质质量分数相等),故填:在t1℃时AB的溶解度相等(t1℃时AB两饱和溶液的溶质质量分数相等);
②t2℃时,A的溶解度是25g,故A的饱和溶液中溶质的质量分数为$\frac{25g}{100g+25g}×100%$=20%,故填:20%;
③A的溶解度随温度的升高而增大,故将t1℃时A的饱和溶液升高温度,溶液中溶质的质量分数不变,故填:不变;
④t2℃时,一小试管内盛有B的饱和溶液,试管底部还存有少许B固体,将小试管放入盛有水的烧杯中,向烧杯中的水中加入一种固体物质X,发现小试管内的固体物质逐渐溶解,说明温度降低,而硝酸铵溶于水温度降低,故填:NH4NO3.
点评 本题考查的是溶解度曲线的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
9.科学探究是我们学习化学的重要方式,实验设计是科学探究的重要环节,下列实验设计能达到实验目的是( )
| A. | 用干燥的红色石蕊试纸检验NH3 | |
| B. | 用紫色石蕊试剂检验烧碱样品是否变质 | |
| C. | 用过量的稀硫酸除去铜粉中混有的镁粉 | |
| D. | 用适量的石灰水除去硫酸钠溶液中混有的碳酸钠 |
6.从2008年6月1日起,在全国实行“限塑令”,禁止生产、销售、使用厚度小于0.025mm的塑料购物袋.下列说法错误的是( )
| A. | 这项措施的实行有助于节能减排 | |
| B. | 塑料购物袋是由合成材料制成的 | |
| C. | 塑料购物袋是造成“白色污染”的来源之一 | |
| D. | 为了防止“白色污染”,将塑料购物袋回收集中烧掉 |
13.某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置,其中过氧化钠可作供氧剂”感到非常好奇,设计实验进行探究.
【提出问题】过氧化钠能与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH=Na2CO3+H2O.用氢氧化钠溶液吸收二氧化碳效果较好.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气.
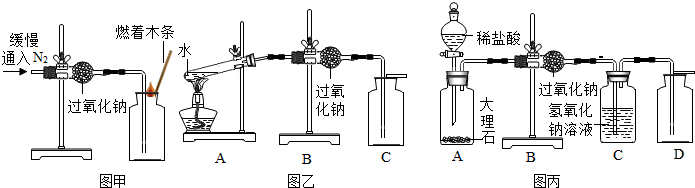
(1)实验操作如图甲所示.
(2)实验现象及结论:观察到燃着木条熄灭现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.
(1)同学们在老师的指导下设计了如图乙所示装置进行实验,并用带火星的木条检验.其中A装置的作用是提供水蒸气.
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气的支持燃烧的性质.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
(1)同学们在老师的指导下设计了如图丙所示装置.
(2)实验记录
【实验反思】
某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.

【提出问题】过氧化钠能与人呼出的哪种气体发生反应?
【查阅资料】①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等.
②CO2+2NaOH=Na2CO3+H2O.用氢氧化钠溶液吸收二氧化碳效果较好.
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
【进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气.
(1)实验操作如图甲所示.
(2)实验现象及结论:观察到燃着木条熄灭现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气.
(1)同学们在老师的指导下设计了如图乙所示装置进行实验,并用带火星的木条检验.其中A装置的作用是提供水蒸气.
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气.实验中这种验证氧气的方法是利用了氧气的支持燃烧的性质.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
(1)同学们在老师的指导下设计了如图丙所示装置.
(2)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | \ | 装置的气密性良好. |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸. | A装置中观察到的现象有有气泡冒出,固体逐渐减少. | A装置中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气.
 人体缺乏维生素C(简称Vc)就会患坏血病,如图所示为某种“维生素C”药片说明书的一部分其中,维生素C“化学式”部分残缺,用“C6H8On”表示.
人体缺乏维生素C(简称Vc)就会患坏血病,如图所示为某种“维生素C”药片说明书的一部分其中,维生素C“化学式”部分残缺,用“C6H8On”表示.  我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某兴趣小组同学从实验室收集到含有碳酸钠和氢氧化钠的混合废液5.44Kg,现用溶质质量分数为19.6%的稀硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某兴趣小组同学从实验室收集到含有碳酸钠和氢氧化钠的混合废液5.44Kg,现用溶质质量分数为19.6%的稀硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求: