题目内容
3.三种无色气体的组成共含有三种元素,现把这三种无色气体组成的混合气体,从A依次通过如图所示的连续装置后,产生实验象如下:
A装置中出白色浑浊;C中有红色物质生成;D中白色粉末变蓝;E中出白色浑浊(以上各步均完全反应).根据上述现象可以判断混合气体的组成是CO2、H2、CO.
分析 根据每个装置中出现的现象和相关物质的性质进行判断.
解答 解:A装置中出白色浑浊,则混合气体中含有CO2气体;B装置中的浓硫酸具有吸水性,干燥空气;C中有红色物质生成,则混合气体中含有还原性气体H2或CO;D中白色粉末变蓝,说明C的反应过程中产生了水,则该混合气体中肯定含有H2;E中出白色浑浊,说明C的反应过程中产生了二氧化碳气体,则混合气体中肯定含有CO.
故答案是:CO2、H2、CO.
点评 本题较难,考查学生气体成分的确定,学生应注意利用气体的性质及检验,明确现象对应的气体检验,并注意物质守恒来推断气体的成分.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.“加碘盐”、“加钙盐”都是以食盐为主原料的调味品.其中“碘”、“钙”泛指( )
| A. | 单质 | B. | 元素 | C. | 分子 | D. | 原子 |
10.下列金属化合物,不能由金属一步转化得到的是( )
| A. | CaCO3 | B. | MgO | C. | FeCl2 | D. | NaOH |
8.某同学想要通过燃烧的方式除去某密闭容器内空气中的氧气,得到较纯净的氮气,下列物质符合要求的是( )
| A. | 石蜡 | B. | 红磷 | C. | 木炭 | D. | 铁丝 |
13. 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).
(1)Na2CO3溶解度曲线为A(填A或B).
(2)Na2CO3俗称纯碱,是一种白色粉末,可以跟CO2和H2O反应生成NaHCO3,该反应的化学方程式为Na2CO3+H2O+CO2=2NaHCO3.
(3)根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是在饱和的碳酸钠溶液中连续通入二氧化碳,可观察到的现是有白色固体析出.
(4)如图2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是A、B和C中的C.
 以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).
以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线(图1).| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(2)Na2CO3俗称纯碱,是一种白色粉末,可以跟CO2和H2O反应生成NaHCO3,该反应的化学方程式为Na2CO3+H2O+CO2=2NaHCO3.
(3)根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是在饱和的碳酸钠溶液中连续通入二氧化碳,可观察到的现是有白色固体析出.
(4)如图2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是A、B和C中的C.

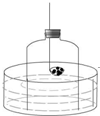 如图所示装置(燃烧匙中盛放的是红磷)可用于实验室测定空气中氧气的含量,将燃烧匙中红磷点燃后迅速伸入玻璃钟罩内,塞紧橡皮塞.根据实验现象回答下列问题:
如图所示装置(燃烧匙中盛放的是红磷)可用于实验室测定空气中氧气的含量,将燃烧匙中红磷点燃后迅速伸入玻璃钟罩内,塞紧橡皮塞.根据实验现象回答下列问题: