题目内容
15.在我国青海湖地区有一种说法,冬天捞碱,夏天晒盐.这里的碱是指Na2CO3,盐是指NaCl.人们从盐湖中捞得的碱含少量的NaCl.某研究性学习小组称取Na2CO3样品(含NaCl)25.0g,将其配制成溶液,再向其中逐滴加入足量的溶质质量分数为7.3%的稀盐酸,使气体完全放出,共收集到8.8gCO2气体,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.求:(1)原固体中Na2CO3的质量分数.
(2)反应中消耗盐酸的总质量.
分析 (1)根据二氧化碳的质量和化学方程式可以计算碳酸钠的质量,然后计算碳酸钠的质量分数;
(2)根据二氧化碳的质量求出盐酸溶液中溶质的质量,然后再计算稀盐酸的总质量.
解答 解:(1)设碳酸钠的质量为x,盐酸溶液中溶质的质量为y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y 8.8g
$\frac{106}{x}=\frac{73}{y}=\frac{44}{8.8g}$
x=21.2g,y=14.6g
所以原固体中碳酸钠的质量分数为:$\frac{21.2g}{25.0g}$×100%=84.8%
(2)反应中消耗盐酸的总质量为:$\frac{14.6g}{7.3%}$=200g
答:(1)原固体中Na2CO3的质量分数为84.8%.
(2)反应中消耗盐酸总质量为200g.
点评 根据化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算出反应中其它物质的质量.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
3.家用电器中常使用大量的印刷电路板,在制电路板时常用氯化铁溶液作为“腐蚀液”.发生反应的化学方程式如下:2FeCl3+Cu=2FeCl2+CuCl2.现向盛有FeCl3溶液的烧杯中,同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )
| A. | 烧杯中有铜、没有铁 | B. | 烧杯中铜、铁都有 | ||
| C. | 烧杯中有铁、没有铜 | D. | 烧杯中铜、铁都没有 |
10.下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
| A. | 氧化铜和炭粉 | B. | 氯化钠和氯化钙 | C. | 水和酒精 | D. | 碳酸钠和碳酸钙 |
20.“伐薪烧炭南山中”是白居易所写的《卖炭翁》中的诗句,而竹炭的吸附能力是木炭的五倍以上,其主要成分竹炭纤维的化学式可表示为(C6H10O5)n.下列说法中,正确的是( )
| A. | 砍伐竹子、烧炭、竹炭净化室内空气都属于物理变化 | |
| B. | 竹炭纤维中C、H、O三种元素的质量比为 36:5:40 | |
| C. | 竹炭的吸附性和可燃性都属于竹炭的化学性质 | |
| D. | 每个(C6H10O5)n分子中含有5n个H2O分子 |
4.用数轴表示某些化学知识直观、简明、易记,下列表示正确的是( )
| A. | 物质形成溶液的pH  | B. | 化合物中氦元素的化合价 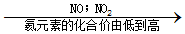 | ||
| C. | 元素在地壳里的含量  | D. | 铁、铜的金属活动性  |