题目内容
18.如图甲为氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验.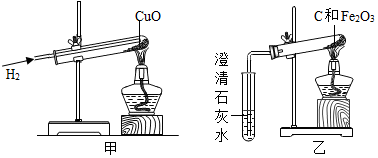
(1)在上述两实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学按照要求规范的进行实验,在实验后发现甲所得的固体中除有一种红色光亮物质外,还有一种砖红色物质.后在查阅有关资料时,找到这样的叙述,氢气还原氧化铜的反应分两步进行:(氧化亚铜为砖红色)
第一步:氢气+氧化铜$\stackrel{△}{→}$氧化亚铜+水 第二步:氢气+氧化亚铜 $\stackrel{△}{→}$铜+水
根据这个知识,请分析该学生在这次实验中所得该砖红色物质的原因可能是①②③(填序号).
①部分氧化铜没有被还原 ②反应中加热时间不够
③停止加热后,铜又被氧化为氧化亚铜
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明反应并没有生成铁.该同学查阅资料,得到铁的氧化物信息如下:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.
分析 (1)在化学反应中得到氧的物质叫还原剂,具有还原性;
(2)根据题干信息来分析解答.
(3)根据“黑色粉末没有溶解,试管中 也未产生预期的气泡,”做出判断;
(4)根据反应物、反应条件、生成物写出化学反应式.
解答 解:(1)氢气和木炭都得到氧是还原剂,具有还原性.
故答案为:还原;
(2)根据题干信息可知,氢气还原氧化铜的过程分为两步进行,则有可能部分氧化亚铜没有被氢气还原为铜,也有可能是加热的时间不够,也有可能反应结束后铜被空气中的氧气氧化为氧化亚铜,故填:①②③.
(3)乙实验完成后,发现澄清石灰水变浑浊,生成部分黑色粉末,黑色粉末是Fe3O4,Fe3O4常温下不溶于稀酸,所以黑色粉末没有溶解,试管中也未产生预期的气泡,说明反应没有发生,无铁单质生成.
故答案为:铁;
(4)碳与氧化铁加热反应生成四氧化三铁和二氧化碳气体,化学反应式是:C+6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+CO2↑.
故答案为:C+6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+CO2↑.
点评 本题考查氢气和碳作还原剂的相关问题,除课本中的相关知识外,还要能从所给的资料中提取信息解决新问题.

练习册系列答案
相关题目
8. 如图为测定空气中氧气含量的实验.下列有关说法正确的是( )
如图为测定空气中氧气含量的实验.下列有关说法正确的是( )
 如图为测定空气中氧气含量的实验.下列有关说法正确的是( )
如图为测定空气中氧气含量的实验.下列有关说法正确的是( )| A. | 红磷燃烧时产生大量的白雾 | |
| B. | 这个实验得到的结论是空气中氧气占$\frac{1}{5}$体积、氮气占$\frac{4}{5}$体积 | |
| C. | 燃烧匙中的红磷不能用木炭代替 | |
| D. | 实验后发现测定的氧气的体积分数低于$\frac{1}{5}$,说明装置一定漏气 |
10.下列水的净化方法中主要是除去水中色素的是( )
| A. | 沉淀 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
7.根据物质的组成,小明将部分物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )
| 类别 | 物质 |
| 甲 | 氯化钠、硫酸铜 |
| 乙 | 盐酸、硫酸 |
| A. | 甲为化合物,乙为单质 | B. | 甲为碱,乙为酸 | ||
| C. | 甲为盐,乙为酸 | D. | 甲为金属,乙为酸 |
8.下列有关物质的性质中,属于化学性质的是( )
| A. | 高锰酸钾是暗紫色固体 | B. | 常温下金属汞是一种液体 | ||
| C. | 甲烷可以在空气中燃烧 | D. | 氧气不易溶于水 |
 小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如图所示,连线表示相互反应).
小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如图所示,连线表示相互反应).