题目内容
8. 如图为测定空气中氧气含量的实验.下列有关说法正确的是( )
如图为测定空气中氧气含量的实验.下列有关说法正确的是( )| A. | 红磷燃烧时产生大量的白雾 | |
| B. | 这个实验得到的结论是空气中氧气占$\frac{1}{5}$体积、氮气占$\frac{4}{5}$体积 | |
| C. | 燃烧匙中的红磷不能用木炭代替 | |
| D. | 实验后发现测定的氧气的体积分数低于$\frac{1}{5}$,说明装置一定漏气 |
分析 在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;④所选除氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态;据此进行分析判断.
解答 解:A、红磷燃烧时产生大量的白烟,而不是白雾,故选项说法错误.
B、冷却至室温,打开弹簧夹,进入集气瓶中的水约占集气瓶容积的$\frac{1}{5}$,这个实验得到的结论是空气中氧气占$\frac{1}{5}$体积,氮气占$\frac{4}{5}$体积,故选项说法正确.
C、木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能用来测定空气中氧气含量,故选项说法错误.
D、实验后发现测定的氧气的体积分数低于$\frac{1}{5}$,也可能是红磷的量不足、未等到装置冷却至室温就打开了弹簧夹等造成的,故选项说法错误.
故选:B.
点评 本题难度不大,掌握测定原理(通过红磷燃烧消耗氧气,导致瓶内压强变小)、实验成功的关键(装置气密性要好;红磷要足量;要冷却到室温再读数)是正确解答此类题的关键.

练习册系列答案
相关题目
9.小胡同学在完成硫酸铜晶体的制备和生长实验时,发现将硫酸铜热饱和溶液冷却到室温,可以观察到( )
| A. | 有白色粉末析出 | B. | 有蓝色晶体析出 | C. | 溶液变为无色 | D. | 溶液变为绿色 |
19.下列属于纯净物的是( )
| A. | 空气 | B. | 矿泉水 | C. | 加碘食盐 | D. | 冰水 |
3.下列关于过氧化氢的组成,叙述正确的是( )
| A. | 过氧化氢是由2个氢原子和2个氧原子组成 | |
| B. | 过氧化氢是由氢分子和氧分子组成 | |
| C. | 过氧化氢是由氢气和氧气组成 | |
| D. | 过氧化氢是由氢元素和氧元素组成 |
20.下列化学用语能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O | B. | Fe | C. | N2 | D. | CO |
17.某研究小组对影响过氧化氢分解反应速率的某些因素进行实验探究.实验记录如表所示.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)该实验的目的是探究过氧化氢溶液的浓度对过氧化氢分解制氧气反应速率的影响.
(3)该实验的结论是H2O2溶液的浓度越高,反应速率越大.
| 实验 序号 | 过氧化氢溶液 的体积(mL) | 过氧化氢溶液 的浓度 | MnO2的质量(g) | 相同时间内收集氧气 的体积(mL) |
| 1 | 50.0 | 1% | 0.1 | 9 |
| 2 | 50.0 | 2% | 0.1 | 16 |
| 3 | 50.0 | 4% | 0.1 | 31 |
(2)该实验的目的是探究过氧化氢溶液的浓度对过氧化氢分解制氧气反应速率的影响.
(3)该实验的结论是H2O2溶液的浓度越高,反应速率越大.
18.如图甲为氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验.
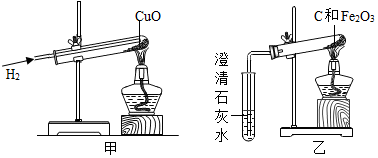
(1)在上述两实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学按照要求规范的进行实验,在实验后发现甲所得的固体中除有一种红色光亮物质外,还有一种砖红色物质.后在查阅有关资料时,找到这样的叙述,氢气还原氧化铜的反应分两步进行:(氧化亚铜为砖红色)
第一步:氢气+氧化铜$\stackrel{△}{→}$氧化亚铜+水 第二步:氢气+氧化亚铜 $\stackrel{△}{→}$铜+水
根据这个知识,请分析该学生在这次实验中所得该砖红色物质的原因可能是①②③(填序号).
①部分氧化铜没有被还原 ②反应中加热时间不够
③停止加热后,铜又被氧化为氧化亚铜
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明反应并没有生成铁.该同学查阅资料,得到铁的氧化物信息如下:
根据以上信息,试写出乙实验试管中反应的化学方程式C+6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+CO2↑,
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.

(1)在上述两实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学按照要求规范的进行实验,在实验后发现甲所得的固体中除有一种红色光亮物质外,还有一种砖红色物质.后在查阅有关资料时,找到这样的叙述,氢气还原氧化铜的反应分两步进行:(氧化亚铜为砖红色)
第一步:氢气+氧化铜$\stackrel{△}{→}$氧化亚铜+水 第二步:氢气+氧化亚铜 $\stackrel{△}{→}$铜+水
根据这个知识,请分析该学生在这次实验中所得该砖红色物质的原因可能是①②③(填序号).
①部分氧化铜没有被还原 ②反应中加热时间不够
③停止加热后,铜又被氧化为氧化亚铜
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明反应并没有生成铁.该同学查阅资料,得到铁的氧化物信息如下:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.
 如图所示,在一个玻璃杯中加入一定量的水,向其中放入一些冰糖,同时在容器外壁标记出液面水平线.
如图所示,在一个玻璃杯中加入一定量的水,向其中放入一些冰糖,同时在容器外壁标记出液面水平线.