题目内容
7.根据物质的组成,小明将部分物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )| 类别 | 物质 |
| 甲 | 氯化钠、硫酸铜 |
| 乙 | 盐酸、硫酸 |
| A. | 甲为化合物,乙为单质 | B. | 甲为碱,乙为酸 | ||
| C. | 甲为盐,乙为酸 | D. | 甲为金属,乙为酸 |
分析 酸是电离时电离出的阳离子全部是氢离子的化合物;由金属离子和酸根离子构成的化合物属于盐,据此分析.
解答 解:甲:氯化钠和硫酸铜都属于化合物的盐;
乙:盐酸和硫酸都属于酸;
故选C.
点评 本题考查物质的分类应用,注意物质组成的分析,概念的实质理解,题目较简单.

练习册系列答案
相关题目
17.某研究小组对影响过氧化氢分解反应速率的某些因素进行实验探究.实验记录如表所示.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)该实验的目的是探究过氧化氢溶液的浓度对过氧化氢分解制氧气反应速率的影响.
(3)该实验的结论是H2O2溶液的浓度越高,反应速率越大.
| 实验 序号 | 过氧化氢溶液 的体积(mL) | 过氧化氢溶液 的浓度 | MnO2的质量(g) | 相同时间内收集氧气 的体积(mL) |
| 1 | 50.0 | 1% | 0.1 | 9 |
| 2 | 50.0 | 2% | 0.1 | 16 |
| 3 | 50.0 | 4% | 0.1 | 31 |
(2)该实验的目的是探究过氧化氢溶液的浓度对过氧化氢分解制氧气反应速率的影响.
(3)该实验的结论是H2O2溶液的浓度越高,反应速率越大.
18.如图甲为氢气和氧化铜反应的实验,图乙是木炭和氧化铁反应的实验.
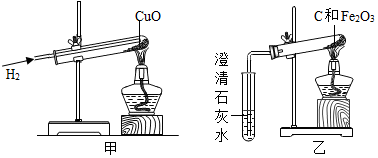
(1)在上述两实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学按照要求规范的进行实验,在实验后发现甲所得的固体中除有一种红色光亮物质外,还有一种砖红色物质.后在查阅有关资料时,找到这样的叙述,氢气还原氧化铜的反应分两步进行:(氧化亚铜为砖红色)
第一步:氢气+氧化铜$\stackrel{△}{→}$氧化亚铜+水 第二步:氢气+氧化亚铜 $\stackrel{△}{→}$铜+水
根据这个知识,请分析该学生在这次实验中所得该砖红色物质的原因可能是①②③(填序号).
①部分氧化铜没有被还原 ②反应中加热时间不够
③停止加热后,铜又被氧化为氧化亚铜
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明反应并没有生成铁.该同学查阅资料,得到铁的氧化物信息如下:
根据以上信息,试写出乙实验试管中反应的化学方程式C+6Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe3O4+CO2↑,
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.

(1)在上述两实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学按照要求规范的进行实验,在实验后发现甲所得的固体中除有一种红色光亮物质外,还有一种砖红色物质.后在查阅有关资料时,找到这样的叙述,氢气还原氧化铜的反应分两步进行:(氧化亚铜为砖红色)
第一步:氢气+氧化铜$\stackrel{△}{→}$氧化亚铜+水 第二步:氢气+氧化亚铜 $\stackrel{△}{→}$铜+水
根据这个知识,请分析该学生在这次实验中所得该砖红色物质的原因可能是①②③(填序号).
①部分氧化铜没有被还原 ②反应中加热时间不够
③停止加热后,铜又被氧化为氧化亚铜
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明反应并没有生成铁.该同学查阅资料,得到铁的氧化物信息如下:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.
12.实验时,若不慎把浓硫酸溅到皮肤上,正确的处理方法是( )
| A. | 立即用水冲洗,再涂上硼酸溶液 | |
| B. | 先用氢氧化钠溶液中和,再用水冲洗 | |
| C. | 先用干布拭干,然后用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液 | |
| D. | 以上处理方法都不正确 |
19.某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示.
请分析上表,并回答下列问题:
(1)该花汁可以(选填“可以”或“不可以”)做酸碱指示剂.
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的肥皂水.
| 试剂 | 稀盐酸 | 食醋 | 蒸馏水 | 肥皂水 | 石灰水 |
| 颜色 | 红 | 红 | 黄 | 绿 | 绿 |
(1)该花汁可以(选填“可以”或“不可以”)做酸碱指示剂.
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的肥皂水.
16.名称中有“水”字的物质可能是溶液,下列有“水”字的物质属于溶液的是( )
| A. | 油水 | B. | 自来水 | C. | 泥水 | D. | 蒸馏水 |
17.假设有(1)Fe、CuS O4、稀H2S O4;(2)CuSO4、KOH、稀HCl;(3)Na2CO3、稀H2SO4、CaCl2三组物质,将它们分别同时放入足量水中,经充分搅拌后静置观察.下列同学们讨论的发言中,正确的是( )
| A. | 只有(1)、(2)组溶液呈蓝色,且一定有沉淀出现 | |
| B. | 只有(1)组液体中,一定有不溶物生成 | |
| C. | 只有(2)、(3)组液体中,可能出现浑浊 | |
| D. | 三组液体中一定都会出现沉淀 |
 如图是用排水法收集到的一瓶无色气体,由此能够确定该气体具有的性质是C
如图是用排水法收集到的一瓶无色气体,由此能够确定该气体具有的性质是C