题目内容
12.某种H2和CO混合气体,其密度是O2的一半,则H2的体积的百分含量为( )| A. | 40% | B. | 46% | C. | 50% | D. | 54% |
分析 由$ρ=\frac{m}{V}=\frac{nM}{nVm}=\frac{M}{Vm}$,摩尔质量与密度呈正比,其密度是氧气的一半,则混合气体的平均摩尔质量是16g/mol,据此列方程式解答即可.
解答 解:混合气体的密度是氧气密度的一半,则混合气体的摩尔质量是16g/mol,设混合气体中含有xmol的氢气,含有ymol的一氧化碳,则有
$\frac{2x+28y}{x+y}=16$
解得:x:y=6:7,
故氢气的体积百分含量为:$\frac{6}{13}×100%$=46%
故选B.
点评 本题考查的是物质的量的计算,侧重于计算能力的考查,注意把握气体的密度与摩尔质量的关系.

练习册系列答案
相关题目
3.下列有关物质的除杂(括号内为杂质)或鉴别所用试剂和方法合理的是( )
| A. | MnO2(KCl)--加水溶解、过滤,蒸发结晶 | |
| B. | 铜粉(CuO)--在氧气流中灼烧 | |
| C. | 鉴别化肥NH4NO3和(NH4)2SO4---取样加熟石灰研磨 | |
| D. | 鉴别羊毛和涤纶----用点燃闻气味的方法 |
9.如表有关物质的除杂、检验、鉴别、分离中所用试剂和方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去氢氧化钠溶液中的碳酸钠 | 加适量氯化钙溶液后过滤 |
| B | 检验生石灰中是否含有石灰石 | 用水或稀盐酸 |
| C | 鉴别化肥氯化铵和氯化钾 | 加熟石灰研磨 |
| D | 分离氯化钠和泥沙的混合物 | 加水溶解后冷却结晶 |
| A. | A | B. | B | C. | C | D. | D |
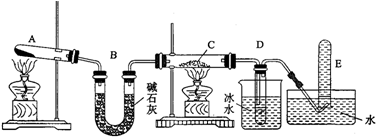
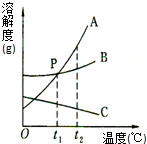 如图是A、B、C三种固体物质的溶解度曲线,请回答:
如图是A、B、C三种固体物质的溶解度曲线,请回答: