题目内容
12.为了测定一批石灰石中碳酸钙的质量分数,某化学兴趣小组同学按下列步骤开展实验:首先将石灰石样品研成粉末,然后取15g石灰石粉末与溶质质量分数10%的稀盐酸恰好完全反应(假设石灰石中的杂质既不与酸反应,也不溶于水),过滤、得到不饱和溶液78.6g.(1)不能用稀硫酸代替盐酸的原因是稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,阻止反应的进行.
(2)求石灰石中碳酸钙的质量分数(保留到0.1%).
分析 碳酸钙和稀硫酸反应生成硫酸钙、水和二氧化碳,生成的硫酸钙微溶于水,包裹在碳酸钙的表面,阻止反应的进行;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的数据可以进行相关方面的计算.
解答 解:(1)因为稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,阻止反应的进行,所以不能用稀硫酸代替盐酸.
故填:稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,阻止反应的进行.
(2)设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x $\frac{73}{100}$x $\frac{44}{100}$x
根据题意有:x+($\frac{73}{100}$x÷10%)-$\frac{44}{100}$x=78.6g,
x=10g,
石灰石中碳酸钙的质量分数为:$\frac{10g}{15g}$×100%=66.7%,
答:石灰石中碳酸钙的质量分数为66.7%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
15.小明和他的同学在实验室发现上一次实验后忘记塞上瓶塞的氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体.他们怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
【讨论】小明同学认为,根据上述实验(1)(2)可推断,猜想②正确.而小张则认为猜想③也可能正确,理由是碳酸钠溶液也能使酚酞溶液变红.
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
12.某种H2和CO混合气体,其密度是O2的一半,则H2的体积的百分含量为( )
| A. | 40% | B. | 46% | C. | 50% | D. | 54% |
7.反应2KMnO4+□X+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O,则下列说法正确的是( )
| A. | 该反应中,X前的化学计量系数为10 | |
| B. | X中所含元素的质量比为1:16 | |
| C. | 反应前后所有元素的化合价都变化了 | |
| D. | 该实验发生装置与实验室用高锰酸钾制氧气的发生装置相同 |
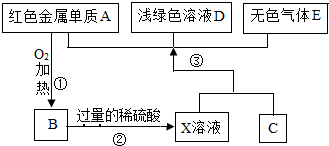 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答: