题目内容
19.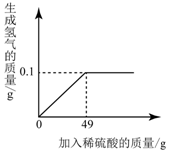 小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:
小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:(1)Cu-Zn合金与纯铜相比,硬度更大的是Cu-Zn合金.
(2)计算稀硫酸溶质的质量分数.
分析 (1)合金的性质是:合金的硬度大,熔点低,耐腐蚀.
(2)根据图中的信息可知氢气的质量.利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出硫酸的质量,进而求出稀硫酸溶质的质量分数.
解答 解:(1)Cu-Zn合金是铜的合金,比纯铜硬度更大;故填:Cu-Zn合金;
(2)由图可知,完全反应后生成氢气的质量为0.1g.
设硫酸的质量为 x
Zn+H2SO4═ZnSO4+H2↑
98 2
x 0.1g
$\frac{98}{x}=\frac{2}{0.1g}$
x=4.9g
稀硫酸溶质的质量分数为$\frac{4.9g}{49g}×100%$=10%;
答:稀硫酸溶质的质量分数为10%.
点评 本题考查根据化学方程式的简单计算,已知生成物的质量求反应物的质量,解题的关键是正确的对图象意义的分析.

练习册系列答案
相关题目
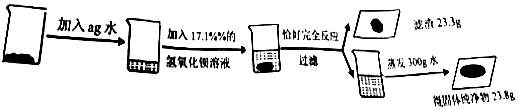
9.某白色固体A可能含有碳酸钠、氧化钙、氯化钠中的一种或几种,进行如下实验:
完成下列问题:
①操作的名称是过滤.根据上述实验多余流程分析,A中一定含有的物质是碳酸钠、氧化钙,C中一定含有的溶质是氢氧化钠.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.

完成下列问题:
①操作的名称是过滤.根据上述实验多余流程分析,A中一定含有的物质是碳酸钠、氧化钙,C中一定含有的溶质是氢氧化钠.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
| 实验操作 | 现象 | 结论 |
| 用一支洁净的试管取适量滤液C,滴加足量稀硝酸和硝酸银溶液. | 产生白色沉淀 | A中有氯化钠 |
10.下表列举了四组待鉴别的物质和对应的鉴别方法,其中不可行的是( )
| 待鉴别的物质 | 鉴别方法 | |
| A | NaOH、NaCl、HCl三种溶液 | 滴入紫色石蕊试液,看颜色 |
| B | 黄金和假黄金(铜锌合金) | 滴加稀盐酸,看是否有气泡产生 |
| C | 烧碱和纯碱 | 滴加澄清石灰水,看是否产生白色沉淀 |
| D | 硬水和软水 | 观察是否澄清 |
| A. | A | B. | B | C. | C | D. | D |
7.化学在工农生产、科技发展和社会生活中发挥着重要作用,下列说法不正确的是( )
| A. | 用铝合金制飞机外壳是因其硬度大、密度小、耐腐蚀 | |
| B. | 发射火箭采用的液氢、液氧都是无污染的纯净物 | |
| C. | 稀有气体通电时会发出各种颜色的光,利用的是其学性质稳定 | |
| D. | 生活中常用加热煮沸的方法降低水的硬度 |
8.用下列方法鉴别物质不能达到实验目的是( )
| 序号 | 实验目的 | 试剂或方法 |
| A | 鉴别FeCl3、NaCl、NaOH、MgCl2四种溶液 | 不另加试剂 |
| B | 鉴别CaCO3、NaCl、NaOH、NH4NO3四种固体粉末 | 水 |
| C | Na2SO4溶液与AgNO3溶液 | 分别加入BaCl2溶液 |
| D | 除去氮气中的少量氧气 | 通过灼热的铜网 |
| A. | A | B. | B | C. | C | D. | D |