题目内容
7.化学在工农生产、科技发展和社会生活中发挥着重要作用,下列说法不正确的是( )| A. | 用铝合金制飞机外壳是因其硬度大、密度小、耐腐蚀 | |
| B. | 发射火箭采用的液氢、液氧都是无污染的纯净物 | |
| C. | 稀有气体通电时会发出各种颜色的光,利用的是其学性质稳定 | |
| D. | 生活中常用加热煮沸的方法降低水的硬度 |
分析 A、根据合金的性质分析解答;
B、根据液氢、液氧的特点分析解答;
C、根据物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质分析解答;
D、根据降低水的硬度的方法解答.
解答 解:A、用铝合金制飞机外壳是因其硬度大、密度小、耐腐蚀,故说法正确;
B、发射火箭采用的液氢、液氧都是无污染的纯净物,故说法正确;
C、稀有气体通电时会发出各种颜色的光,不需要发生化学变化就能表现出来,是利用了其物理性质,故说法错误;
D、生活中常用加热煮沸的方法降低水的硬度,故说法正确;
故选C.
点评 本题考查的是化学与生活的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
15.实验室用铜辉矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备某种碱式碳酸铜【Cua(OH)b(CO3)c•dH2O】的主要实验流程如下.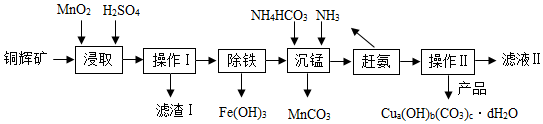
(1)操作I和操作II中玻璃棒的作用是引流.
(2)“浸取”步骤中发生反应(I、II),其中反应I为:2MnO2+Cu2S+□H2SO4=2MnSO4+2CuSO4+S↓+4H2O,请在□中填上合适的化学计量数为4.
(3)“浸取”步骤中,另一反应II为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(4)滤渣I的成分为MnO2、S、SiO2等杂质.
(5)已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
“除铁”步骤中,控制适宜的pH范围为2.7~3.2.

(1)操作I和操作II中玻璃棒的作用是引流.
(2)“浸取”步骤中发生反应(I、II),其中反应I为:2MnO2+Cu2S+□H2SO4=2MnSO4+2CuSO4+S↓+4H2O,请在□中填上合适的化学计量数为4.
(3)“浸取”步骤中,另一反应II为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(4)滤渣I的成分为MnO2、S、SiO2等杂质.
(5)已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀 | 7.5 | 2.7 | 5.2 | 8.3 |
| 完全沉淀 | 9.7 | 3.2 | 6.4 | 9.8 |
2.生活中充满变化.下列选项中不涉及化学变化的是( )
| A. | 浓盐酸敞口放置,在空气中形成“白雾” | |
| B. | 用食醋除去水壶中的水垢 | |
| C. | 二氧化碳作气体肥料 | |
| D. | 高炉炼铁 |
 如图所示的是初中化学中的一些重要实验.请回答下列问题:
如图所示的是初中化学中的一些重要实验.请回答下列问题:
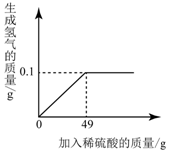 小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:
小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算: 小明同学绘制了如图所示A、B两种固体物质的溶液度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶液度曲线: