题目内容
4.水和溶液在生命活动和生活中起着十分重要的作用
(1)自然界的水常常遭到人为污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指C(填字母).
A、分子 B、原子 C、元素 D、单质
(2)水在化学实验中的作用不可忽视,如图1中五个实验分别用到水.下列说法中正确的是①③(填序号)
①实验A中水作溶剂.
②实验B中水的作用是吸收生成物,防止生成物扩散到空气中污染大气.
③实验C中通过烧杯中水进入集气瓶中的体积可得出氧气约占空气总体积$\frac{1}{5}$的结论
④实验D中水的作用只是提供热量.
⑤实验E中的水仅作反应物.
(3)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂,受热时发生如下反应:4K2FeO4$\frac{\underline{\;\;△\;\;}}{\;}$aR+4K2O+3O2↑,则a、R分别是B(填字母).
A.4 FeO B.2 Fe2O3 C.3 Fe2O3 D.1 Fe3O4
(4)甲、乙、丙三种固体物质的溶解度曲线如图2所示,回答下列问题:
①t2℃时,甲、乙、丙三物质的溶解度由大到小的顺序是丙>甲>乙.
②t2℃时,将20g甲投入50g水中,充分溶解后形成溶液的溶质质量分数为23.1%(保留0.1%).
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别同时降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是丙>甲>乙.
分析 根据物质是由元素组成的解答,根据实验中水的作用解答;根据质量守恒定律化学反应前后原子的种类和原子的个数不变解答;根据溶解度曲线以及意义进行分析解答即可.
解答 解:(1)污染物中氮和磷是物质的组成元素,故填:C;
(2)根据图示可以看出,①实验A中水作溶剂,正确.②实验B中水的作用是防止高温熔化物溅落炸裂瓶底,错误.③实验C中通过烧杯中水进入集气瓶中的体积可得出氧气约占空气总体积$\frac{1}{5}$的结论,正确.④实验D中水的作用除了提供热量还能起到隔绝氧气的作用,错误.⑤实验E中的水除了作反应物还能作溶剂,错误.故填:①③;
(3)4K2FeO4$\frac{\underline{\;\;△\;\;}}{\;}$aR+4K2O+3O2↑,根据反应可以看出,R中含有铁元素和氧元素,生成物中含有10个O原子,反应物中含有16个氧原子,故aR中含有6个O原子,反应物中含有4个Fe原子,故aR中含有4个Fe原子,因此a是2,R是Fe2O3,故填:B;
(4)①根据图象可以看出,t2℃时,甲、乙、丙三物质的溶解度由大到小的顺序是丙>甲>乙,故填:丙>甲>乙.
②t2℃时,甲的溶解度为30g,故将20g甲投入50g水中,充分溶解后,只能溶解15g,故形成溶液的溶质质量分数为$\frac{15g}{50g+15g}×100%≈$ 23.1%,故填:23.1%.
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别同时降温至t2℃,甲和乙的溶解度减小,根据t2℃时的溶解度可以看出,甲的溶解度大于乙,故甲的溶质质量分数大于乙,丙的溶解度随温度的降低而减小,溶质质量分数不变,根据图象可以看出,丙的溶质质量分数大于甲,故所得溶液中溶质质量分数由大到小的顺序是丙>甲>乙,故填:丙>甲>乙.
点评 本题考查的是水的有关应用以及溶解度曲线的应用的知识,完成此题,可以依据已有的知识进行.

| A. | 秋收后,秸秆应尽快焚烧,避免占用耕地 | |
| B. | 大力推广燃气汽车和电动汽车,改变能源结构 | |
| C. | 工地施工时,要既是洒水减少建筑扬尘 | |
| D. | 汽车尾气、化石燃料的燃烧都是雾霾产生的原因 |
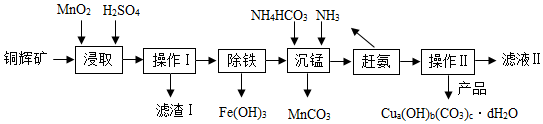
(1)操作I和操作II中玻璃棒的作用是引流.
(2)“浸取”步骤中发生反应(I、II),其中反应I为:2MnO2+Cu2S+□H2SO4=2MnSO4+2CuSO4+S↓+4H2O,请在□中填上合适的化学计量数为4.
(3)“浸取”步骤中,另一反应II为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(4)滤渣I的成分为MnO2、S、SiO2等杂质.
(5)已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀 | 7.5 | 2.7 | 5.2 | 8.3 |
| 完全沉淀 | 9.7 | 3.2 | 6.4 | 9.8 |
 如图所示.瓶中X为固体.当把滴管内的液体Y滴入瓶中.导管口一定没有气泡生的是( )
如图所示.瓶中X为固体.当把滴管内的液体Y滴入瓶中.导管口一定没有气泡生的是( ) | A | B | C | D | |
| X | MnO2 | NH4NO3 | CaO | CaCO3 |
| Y | H2O2 | H2O | H2O | HCl |

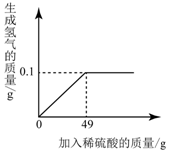 小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算:
小王同学想测定某Cu-Zn合金中铜的质量分数,取一定量合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所用稀硫酸与生成氢气的质量关系如图所示.请完成下列分析及计算: 某兴趣小组用10g镁条与一定溶质质量分数的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图所示(假设镁条中除表面含有氧化镁外.没有其他杂质)
某兴趣小组用10g镁条与一定溶质质量分数的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图所示(假设镁条中除表面含有氧化镁外.没有其他杂质) 小明同学绘制了如图所示A、B两种固体物质的溶液度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶液度曲线: 随意丢弃废旧干电池会造成严重的环境污染,而废旧干电池中许多物质都可以再回收利用.请根据图回答下列问题.
随意丢弃废旧干电池会造成严重的环境污染,而废旧干电池中许多物质都可以再回收利用.请根据图回答下列问题.