题目内容
请按照要求写出下列化学方程式.
(1)木炭还原氧化铜 ;
(2)实验室制取二氧化碳 .
(1)木炭还原氧化铜
(2)实验室制取二氧化碳
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)木炭还原氧化铜,可知反应物木炭和氧化铜,生成物为铜和二氧化碳,则可书写化学方程式;
(2)实验室制取CO2的反应原理是大理石(或石灰石)与稀盐酸反应生成氯化钙、水和二氧化碳.
(2)实验室制取CO2的反应原理是大理石(或石灰石)与稀盐酸反应生成氯化钙、水和二氧化碳.
解答:解:
(1)由题意可知反应物木炭和氧化铜,生成物为铜和二氧化碳,故C+2CuO
2Cu+CO2↑;
(2)实验室制取CO2的反应原理是大理石(或石灰石)与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
答案:
(1)C+2CuO
2Cu+CO2↑;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑.
(1)由题意可知反应物木炭和氧化铜,生成物为铜和二氧化碳,故C+2CuO
| ||
(2)实验室制取CO2的反应原理是大理石(或石灰石)与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
答案:
(1)C+2CuO
| ||
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评:学会理论联系实际,学习化学,应用于生活;根据质量守恒定律,正确书写化学方程式.

练习册系列答案
相关题目
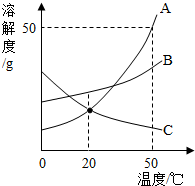 如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )| A、除去A中混油的少量的B,可采用降温结晶的方法 |
| B、50℃时A的饱和溶液中,溶质的质量分数为50% |
| C、将C的饱和溶液变为不饱和溶液,可采用升高温度的方法 |
| D、将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=B |
 近来中国部分地区出现镉污染的大米,食用后对人体有害.下图甲为元素周期表中的镉元素,图乙为镉原子结构示意图.请回答:
近来中国部分地区出现镉污染的大米,食用后对人体有害.下图甲为元素周期表中的镉元素,图乙为镉原子结构示意图.请回答:
 同学设计的实验装置(如右图),既可用于制取气体,又可用于验证物质性质.
同学设计的实验装置(如右图),既可用于制取气体,又可用于验证物质性质.