题目内容
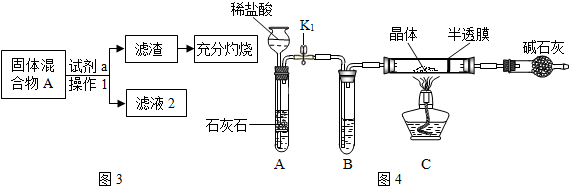
实验室可用下图装置模拟工业炼铁.

(1)一氧化碳与氧化铁(Fe2O3)反应的化学方程式是 .
(2)实验前先通入CO的目的是 试管中出现的现象是
(3)装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是 .

(1)一氧化碳与氧化铁(Fe2O3)反应的化学方程式是
(2)实验前先通入CO的目的是
(3)装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是
考点:一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据反应物生成物及反应条件写出化学方程式;
(2)根据一氧化碳的可燃性及实验现象分析;
(3)根据一氧化碳的毒性分析.
(2)根据一氧化碳的可燃性及实验现象分析;
(3)根据一氧化碳的毒性分析.
解答:解:(1)一氧化碳与氧化铁反应生成铁和二氧化碳,化学方程式为3CO+Fe2O3
2Fe+3CO2;
(2)一氧化碳具有可燃性,点燃不纯的一氧化碳可能发生爆炸,因此实验前要先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸,加热时红色的氧化铁粉末变成黑色,生成的二氧化碳使试管内澄清石灰水变浑浊;
(3)一氧化碳有毒,不能直接排放到空气中,因此要在装置图末端的导气管口放一盏燃着的酒精灯将一氧化碳燃烧除去,防止污染空气;
故答案为:(1)3CO+Fe2O3
2Fe+3CO2;
(2)排净装置内的空气,防止加热时发生爆炸;澄清石灰水变浑浊;
(3)用点燃法去掉一氧化碳,防止污染空气.
| ||
(2)一氧化碳具有可燃性,点燃不纯的一氧化碳可能发生爆炸,因此实验前要先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸,加热时红色的氧化铁粉末变成黑色,生成的二氧化碳使试管内澄清石灰水变浑浊;
(3)一氧化碳有毒,不能直接排放到空气中,因此要在装置图末端的导气管口放一盏燃着的酒精灯将一氧化碳燃烧除去,防止污染空气;
故答案为:(1)3CO+Fe2O3
| ||
(2)排净装置内的空气,防止加热时发生爆炸;澄清石灰水变浑浊;
(3)用点燃法去掉一氧化碳,防止污染空气.
点评:本题考查一氧化碳还原氧化铁的原理、实验现象及操作注意事项,要根据已有的知识进行分析解答.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目