题目内容
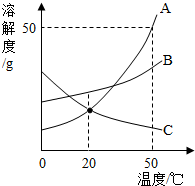 如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法正确的是( )| A、除去A中混油的少量的B,可采用降温结晶的方法 |
| B、50℃时A的饱和溶液中,溶质的质量分数为50% |
| C、将C的饱和溶液变为不饱和溶液,可采用升高温度的方法 |
| D、将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=B |
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据A、B的溶解度随温度的变化情况分析分离混合物的方法;
B、根据50℃时A的溶解度计算分析;
C、根据C的溶解度随温度的变化情况分析;
D、根据A、B、C三种物质的溶解度随温度变化的趋势及在50℃、20℃时溶解度的大小分析比较.
B、根据50℃时A的溶解度计算分析;
C、根据C的溶解度随温度的变化情况分析;
D、根据A、B、C三种物质的溶解度随温度变化的趋势及在50℃、20℃时溶解度的大小分析比较.
解答:解:A、由A、B两种物质的溶解度曲线可知,A物质的溶解度手温度的影响较大,B物质的溶解度受温度的影响不大,除去A中混油的少量的B,可采用降温结晶的方法,故A正确;
B、由A的溶解度曲线可知,在50℃时A的溶解度是50g,A的饱和溶液中溶质的质量分数为:
×100%=33.3%.故B错误;
C、由C固体物质的溶解度曲线图可知,C物质的溶解度随温度的升高而降低.所以,从改变温度的角度考虑,要使C物质接近饱和的溶液变为饱和溶液,应采取的措施是升高温度.故C错误;
D、由A、B、C三种物质的溶解度曲线可知,A、B的溶解度随温度的升高而增大,C的溶解度随温度的升高而降低.将50℃时三种物质的饱和溶液降温至20℃,A、B的饱和溶液有晶体析出,形成了20℃的饱和溶液,C的饱和溶液转变为不饱和溶液.由于在20℃时,B的溶解度大于A的溶解度且都大于在50℃时C的溶解度.所以,将50℃时三种物质的饱和溶液降温至20℃时,三种物质溶液中溶质的质量分数由大到小的顺序是:B>A>C.故D错误.
故选:A.
B、由A的溶解度曲线可知,在50℃时A的溶解度是50g,A的饱和溶液中溶质的质量分数为:
| 50g |
| 50g+100g |
C、由C固体物质的溶解度曲线图可知,C物质的溶解度随温度的升高而降低.所以,从改变温度的角度考虑,要使C物质接近饱和的溶液变为饱和溶液,应采取的措施是升高温度.故C错误;
D、由A、B、C三种物质的溶解度曲线可知,A、B的溶解度随温度的升高而增大,C的溶解度随温度的升高而降低.将50℃时三种物质的饱和溶液降温至20℃,A、B的饱和溶液有晶体析出,形成了20℃的饱和溶液,C的饱和溶液转变为不饱和溶液.由于在20℃时,B的溶解度大于A的溶解度且都大于在50℃时C的溶解度.所以,将50℃时三种物质的饱和溶液降温至20℃时,三种物质溶液中溶质的质量分数由大到小的顺序是:B>A>C.故D错误.
故选:A.
点评:掌握固体溶解度曲线的变化趋势及其作用;了解溶质的质量分数、溶解性和溶解度的关系是解答本题关键.

练习册系列答案
相关题目
硅酸钠(Na2SiO3)可用作粘合剂和防火材料.硅酸钠中硅元素的化合价为( )
| A、+l | B、+2 | C、+3 | D、+4 |
如图表示一个化学反应微观变化的情况,其中不同的圆球代表不同种元素原子.下列说法不正确的是( )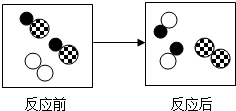

| A、此反应有单质生成 |
| B、分子在化学变化中是不可分的 |
| C、该反应是置换反应 |
| D、参加反应的两种分子的个数比为2:1 |
造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
| A、分子很小 |
| B、分子在不断运动 |
| C、分子之间有间隔 |
| D、分子间有相互作用 |
装修房屋用到的下列材料,属于有机合成材料的是( )
| A、大理石 | B、沙土 |
| C、铝合金 | D、塑料水管 |
下列对水的描述中不正确的( )
| A、水由水分子构成 |
| B、水分子由氢原子和氧原子构成 |
| C、水由氢元素和氧元素组成 |
| D、水由氢气和氧气组成 |