题目内容
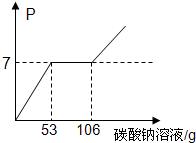 取20g含HCl和CaCl2的溶液,向其中加入10%的碳酸钠溶液,加入碳酸钠溶液的质量与溶液pH的变化关系如图所示.
取20g含HCl和CaCl2的溶液,向其中加入10%的碳酸钠溶液,加入碳酸钠溶液的质量与溶液pH的变化关系如图所示.(1)求生成二氧化碳的质量.
(2)求生成沉淀的质量.
(3)计恰好完成反应时所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据碳酸钠溶液质量、质量分数可以计算生成二氧化碳的质量、沉淀碳酸钙的质量;
加入106g碳酸钠溶液时恰好完全反应,根据碳酸钠溶液质量、质量分数可以计算生成氯化钠的质量,进一步可以计算恰好完成反应时所得溶液中溶质的质量分数.
加入106g碳酸钠溶液时恰好完全反应,根据碳酸钠溶液质量、质量分数可以计算生成氯化钠的质量,进一步可以计算恰好完成反应时所得溶液中溶质的质量分数.
解答:解:(1)设生成二氧化碳的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
53g×10% y x
=
=
,
x=2.2g,y=5.85g,
答:生成二氧化碳的质量是2.2g.
(2)设生成沉淀的质量为z,生成氯化钠的质量为m,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
(106g-53g)×10% z m
=
=
,
z=5g,m=5.85g,
答:生成沉淀的质量是5g.
(3)恰好完成反应时所得溶液中溶质的质量分数为:
×100%=9.8%,
答:恰好完成反应时所得溶液中溶质的质量分数为9.8%.
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
53g×10% y x
| 106 |
| 53g×10% |
| 117 |
| y |
| 44 |
| x |
x=2.2g,y=5.85g,
答:生成二氧化碳的质量是2.2g.
(2)设生成沉淀的质量为z,生成氯化钠的质量为m,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
(106g-53g)×10% z m
| 106 |
| (106g-53g)×10% |
| 100 |
| z |
| 117 |
| m |
z=5g,m=5.85g,
答:生成沉淀的质量是5g.
(3)恰好完成反应时所得溶液中溶质的质量分数为:
| 5.85g+5.85g |
| 20g+106g-5g-2.2g |
答:恰好完成反应时所得溶液中溶质的质量分数为9.8%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列做法中,不利于保护水资源的是( )
| A、使用节水型马桶 |
| B、使用含磷洗衣粉 |
| C、合理使用农药和化肥 |
| D、工业废水处理达标后排放 |
下列各组物质间通过一步反应就能实现如图转化,则甲、乙、丙可能是( )


| A、H2O2、H2O、O2 |
| B、C、CO、CO2 |
| C、CaO、Ca(OH)2、CaCO3 |
| D、NaOH NaCl NaNO3 |




 甲、乙两种晶体(不含结晶水)的溶解度曲线如图所示.
甲、乙两种晶体(不含结晶水)的溶解度曲线如图所示.