题目内容
某化学兴趣小组的同学对一份固体样品进行了探究.通过实验已确定该样品由氧化铁和铁粉混合而成.他们称取了13.6g固体样品,用图1所示的装置继续实验,测定的部分数据如图2所示.
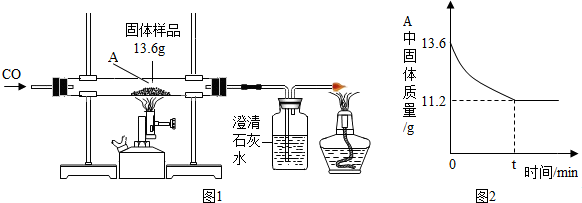
请计算:固体样品中氧化铁的质量是多少?

请计算:固体样品中氧化铁的质量是多少?
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:反应前后固体质量减少的部分是氧化铁中氧元素的质量,根据氧元素的质量可以计算氧化铁的质量.
解答:解:方法一:设固体样品中氧化铁的质量为x,
氧化铁中氧元素的质量为:13.6g-11.2g=2.4g,
则有:x×
×100%=2.4g,
x=8g,
答:固体样品中氧化铁的质量是8g.
方法二:设固体样品中氧化铁的质量为y,
Fe2O3+3CO
2Fe+3CO2,△m
160 112 160-112=48
=
,
y=8g,
答:固体样品中氧化铁的质量是8g.
氧化铁中氧元素的质量为:13.6g-11.2g=2.4g,
则有:x×
| 48 |
| 160 |
x=8g,
答:固体样品中氧化铁的质量是8g.
方法二:设固体样品中氧化铁的质量为y,
Fe2O3+3CO
| ||
160 112 160-112=48
| 160 |
| 48 |
| y |
| 13.6g-11.2g |
y=8g,
答:固体样品中氧化铁的质量是8g.
点评:本题主要考查学生运用假设法进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
下列说法正确的是( )
| A、氧化物都是含氧元素的化合物 |
| B、分子是化学变化中的最小微粒 |
| C、有单质生成的反应都是置换反应 |
| D、电解水时负极产生的气体是氧气 |
下列金属中,活动性最强的是( )
| A、镁 | B、铁 | C、铜 | D、锌 |
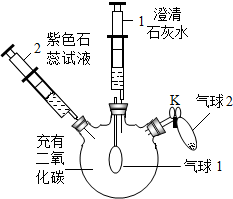


 现有A、B、C、D、E五种物质,分别为铁、氧化钙、盐酸、氢氧化钙和硫酸铜中的一种.
现有A、B、C、D、E五种物质,分别为铁、氧化钙、盐酸、氢氧化钙和硫酸铜中的一种.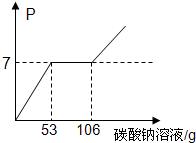 取20g含HCl和CaCl2的溶液,向其中加入10%的碳酸钠溶液,加入碳酸钠溶液的质量与溶液pH的变化关系如图所示.
取20g含HCl和CaCl2的溶液,向其中加入10%的碳酸钠溶液,加入碳酸钠溶液的质量与溶液pH的变化关系如图所示.