题目内容
20.某学生为了测定由两种元素形成的气态化合物X的组成,做了如下图所示的实验.他把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应,得到如下结果: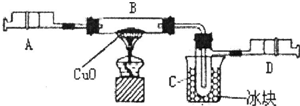
①实验前B管和药品的总质量为21.32g,实验后为21.16g.
②C管中收集到的物质电解后得到H2和O2,在D中收集到的是N2.
③X中两元素的质量比是14:3.
问:(1)C中收集到的液体,质量是0.18g,
(2)在实验中看到的现象是B管中固体由黑变红,C管中有液体出现.
(3)B中反应的化学方程式是2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu十N2+3H2O.
分析 装置B中氧化铜变为铜,所以减少的质量为氧化铜中氧元素的质量,而氧元素又与氨气中的氢元素接合成水,所以水中氧元素的质量与水中氧元素的质量相等.从而求出水的质量.
解答 解:(1)C中收集到的水的质量为:(21.32g-21.16g)÷$\frac{16}{18}$×100%=0.18g,故填:0.18;
(2)氧化铜与氨气反应生成铜和水和氮气.所以现象为黑色固体逐渐变为红色.C管中有无色液体出现;D的内管向外推动.故填:B管中固体由黑变红,C管中有液体出现;
(3)B中是氨气与氧化铜反应生成铜、氮气和水,其化学方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu十N2+3H2O;故填:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu十N2+3H2O.
点评 本题考查的是物质成分的确定以及化学方程式书写的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
12.实验是研究化学的重要方法,以下实验不正确的是( )
| A. | 用点燃的方法除去二氧化碳中混有的少量的一氧化碳 | |
| B. | 用带火星的木条鉴别氧气和空气 | |
| C. | 用碘水或碘酒检验火腿肠中是否含有淀粉 | |
| D. | 配制10%氯化钠溶液的一般步骤是:计算、称量、溶解 |
11.某元素R形成的含氧酸盐的化学式为Nan+1RO2n+2,其中的n值可能是( )
| A. | 1或2 | B. | 2或3 | C. | 0或3 | D. | 0或1 |
9.含硫化氢(H2S)的工业废气排入空气会造成污染.可采用NaOH溶液进行吸收,同时可以制得某种可溶性化合物Y,反应的化学方程式为H2S+2NaOH=Y+2H2O,工艺流程图如下图所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 硫化氢溶液的酸碱度可用石蕊试液测定 | |
| B. | “系列操作”中一定有过滤的操作 | |
| C. | Y的化学式为Na2SO4 | |
| D. | 吸收H2S的反应是中和反应 |
10.下列有关二氧化碳说法正确的是( )
| A. | 二氧化碳可用排水法收集 | |
| B. | 二氧化碳可用燃着的木条鉴定 | |
| C. | 二氧化碳在实验室可以用块状石灰石和浓硫酸反应制备 | |
| D. | 干冰用于制造舞台云雾是因为干冰易升华吸热 |

