题目内容
1.在氮的氧化物中,测得氮、氧两种元素的质量比为7:12,则该氧化物是( )| A. | N2O5 | B. | N2O3 | C. | N2O | D. | NO2 |
分析 由题意,氮、氧两种元素的质量比为7:12,据此结合化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:在氮的氧化物中,测得氮、氧两种元素的质量比为7:12,则该化合物的分子中氮原子和氧原子的个数比为$\frac{7}{14}$:$\frac{12}{16}$=2:3,则该化合物的化学式为:N2O3.
故选:B.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
10.化石燃料是不可再生能源,在地球上蕴藏量是有限的,开发和有效利用新能源迫在眉睫.下列能源中属于新能源的是( )
| A. | 煤 | B. | 潮汐能 | C. | 石油 | D. | 天然气 |
11.除去下列各物质中混有的少量杂质,所用试剂及操作方法均正确的是( )
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | H2 | HCl | 通过足量的NaOH溶液,干燥 |
| B | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,过滤 |
| C | NaCl固体 | Na2CO3 | 加入足量水溶解,过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
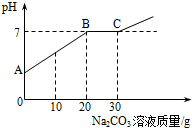 向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题:
向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题: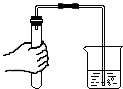 如图所示装置,如何检验装置的气密性?
如图所示装置,如何检验装置的气密性?